

| A. | 在(t1+10)min时,其他条件不变,增大压强,平衡向逆反应方向移动 | |
| B. | (t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向右移动 | |
| C. | T℃时,在相同容器中,若由0.3 mol•L-1 A、0.1 mol•L-1 B和0.4 mol•L-1C反应,达到平衡后,C的浓度仍为0.4 mol•L-1 | |
| D. | 该反应为吸热反应,温度升高,平衡正向移动,A的转化率升高 |
分析 该反应达到平衡状态时,A浓度的变化量=(0.5-0.3)mol/L=0.2mol/L,B浓度的变化量=(0.7-0.1)mol/L=0.6mol/L,C浓度的变化量=(0.4-0)mol/L=0.4mol/L,同一化学反应同一时间段内,各物质浓度的变化量之比等于其计量数之比,所以该反应方程式为:A(g)+3B(g)?2C(g),根据“先拐先平数值大”结合图II知,T1>T2,升高温度,B的体积发生增大,则该反应的正反应是放热反应,据平衡的建立以及平衡的移动知识来回答.
解答 解:反应达到平衡状态时,A浓度的变化量=(0.5-0.3)mol/L=0.2mol/L,B浓度的变化量=(0.7-0.1)mol/L=0.6mol/L,C浓度的变化量=(0.4-0)mol/L=0.4mol/L,同一化学反应同一时间段内,各物质浓度的变化量之比等于其计量数之比,所以该反应方程式为:A(g)+3B(g)?2C(g),
根据“先拐先平数值大”结合图Ⅱ知,T1>T2,升高温度,B的体积发生增大,则该反应的正反应是放热反应;
A.该反应的正反应是气体体积减小的反应,t2时,保持其它条件和物质状态不变,增加压强,化学平衡向正反应方向移动,故A错误;
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,体积增大,相当于减小了压强,所以平衡逆向移动,故B错误;
C.T℃时,在相同容器中,若由0.3 mol•L-1 A、0.1 mol•L-1 B和0.4 mol•L-1C反应,将C转化为反应物,则A的是0.5mol/L,B的是0.7mol/L,所以和开始的投料一样,建立的平衡是等同的,所以达到平衡后,C的浓度仍为0.4 mol/L,故C正确;
D.其它条件不变,升高温度,正逆反应速率都增大,平衡向吸热反应方向移动,根据图Ⅱ知,正反应是放热反应,所以平衡向逆反应方向移动,A的转化率降低,故D错误;
故选:C.
点评 本题考查外界条件对化学平衡移动的影响,正确确定反应方程式是解本题关键,会根据“先拐先平数值大”确定该反应是吸热反应还是放热反应,难度中等.


科目:高中化学 来源: 题型:解答题
 某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏水洗净滴定管后,装入标准盐酸进行滴定 | |
| B. | 用蒸馏水冼净锥形瓶后,再用NaOH液润洗,而后装入一定体积的NaOH溶液 | |
| C. | 滴定前平视滴定管刻度线,滴定终了俯视刻度线 | |
| D. | 滴定前酸式滴定管尖嘴部分有气泡,滴定终了无气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | s轨道呈球形,p轨道呈哑铃形 | B. | Cu元素在元素周期表的d区 | ||
| C. | 12g二氧化硅中有0.8NA个Si-O键 | D. | H2O中O原子的杂化方式是sp3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 2,4-二甲基已烷
2,4-二甲基已烷 3-甲基-1-丁烯
3-甲基-1-丁烯



 +3HO-NO2
+3HO-NO2
 +3H2O
+3H2O CH2=CHCl.
CH2=CHCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. )不能与强碱性物质混合使用,其原因是
)不能与强碱性物质混合使用,其原因是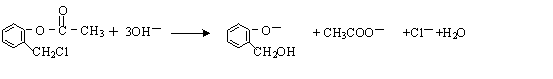 (写离子方程式).
(写离子方程式). )通过加成、取代等一系列转化合成某高分子化合物
)通过加成、取代等一系列转化合成某高分子化合物
 、
、 、
、 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
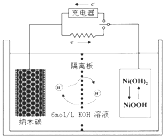 据新华社2009年5月9日电,国务院总理温家宝主持召开国务院常务会议,会上通过了我国2009年将投入大量资金发展新能源汽车,支持节能、环保、安全等关键技术开发,为我国社会经济可持续发展打下良好基础,为今后改善环境、提升民众的生活质量具有极为重要的意义.请回答下列问题:
据新华社2009年5月9日电,国务院总理温家宝主持召开国务院常务会议,会上通过了我国2009年将投入大量资金发展新能源汽车,支持节能、环保、安全等关键技术开发,为我国社会经济可持续发展打下良好基础,为今后改善环境、提升民众的生活质量具有极为重要的意义.请回答下列问题:| 物质 | H2 | CO | CH4 |
| 热值/kJ•g-1 | 143 | 10 | 56 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com