
下列实验操作中错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 蒸馏中,冷却水应从冷凝管的下口通入,上口流出
D. 过滤操作时,漏斗颈下端不能紧靠烧杯内壁
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学卷(解析版) 题型:选择题
一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2。符合上述转化关系的A、C可能是

①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2
A.只有②③④⑥ B.除①外 C.除⑤外 D.全部
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学卷(解析版) 题型:选择题
关于下图所示①、②两个装置的叙述中,正确的是( )

A.硫酸浓度变化:①增大,②减小
B.装置名称:①是原电池,②是电解池
C.电极反应式:①中阳极:4OH--4e-=2H2O+O2↑;②中正极:Zn-2e-===Zn2+
D.离子移动方向:①中H+向阴极方向移动,②中H+向负极方向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高一阶段考一化学卷(解析版) 题型:实验题
①在过滤时需要用到的有 (填序号,下同)。
②在蒸馏时需要用到的有 。
③在萃取时需要用到的有 。
④在蒸发结晶时需要用到的有 。
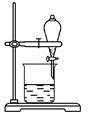
(2)用CCl4萃取碘水中的碘在右图的分液漏斗中,下层液体呈________色;他们打开分液漏斗活塞,却未见液体流下,原因可能是______________________。
(3)某同学用某种粗盐进行提纯实验,步骤见下图。
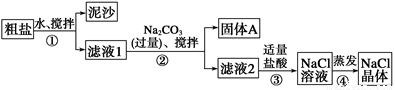
请回答下列问题:
①步骤①和②的操作名称是________。
②步骤③判断加入盐酸“适量”的方法是______________;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止____________,当蒸发皿中有较多量固体出现时,应________,用余热使水分蒸干。
③猜想和验证:
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | _________ | 猜想Ⅰ成立 |
猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入__________,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | ___________ |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,____________ | _________ | 猜想Ⅲ成立 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高一阶段考一化学卷(解析版) 题型:选择题
同温同压下,等质量的SO2与SO3相比较,下列叙述正确的( )
A.分子个数比为4∶5 B.含硫元素质量比为4∶5
C.含氧原子个数比为5∶6 D.含硫原子个数比为5∶6
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高一阶段考一化学卷(解析版) 题型:选择题
现有下列仪器:①集气瓶;②量筒;③烧杯;④表面皿;⑤蒸发皿;⑥容量瓶;⑦圆底烧瓶。其中能用酒精灯加热的是( )
A. ①③④ B. ②③⑤ C. ③⑤⑦ D. ③⑥⑦
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上第一次月考化学卷(解析版) 题型:实验题
(1)配制240mL0.1mol/L的盐酸溶液,应量取盐酸体积 mL,实验中用到的仪器除了烧杯、玻璃棒、量筒外还有:
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏高的是________
A.摇匀后静置,发现液面低于刻度线,继续加水至与刻度线相切
B.量取浓盐酸时俯视读数
C.定容时仰视
D.在配制前用已知浓度的稀盐酸润洗容量瓶
E.洗涤量取浓盐酸的量筒,并将洗涤液一并转入烧杯中
F.溶液没有恢复到室温就进行定容
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上第一次月考化学卷(解析版) 题型:选择题
下列 除杂试剂或操作方法不正确的是( )
除杂试剂或操作方法不正确的是( )
选项 | 物质 | 杂质 | 除杂试剂或操作方法 |
A | KNO3溶液 | KOH | 加入适量FeCl3溶液,过滤 |
B | H2 | CO2 | 先后通过盛NaOH溶液、浓硫酸的洗气瓶 |
C | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
D | FeSO4溶液 | CuSO4 | 加入过量铁粉,过滤 |
查看答案和解析>>
科目:高中化学 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
一定条件下,可逆反应的平衡常数可以用平衡浓度计算, 也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是
也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是
A.对于C2H4(g)+H2O(g)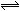 C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则用分压表示的平衡常数KP=3/P
C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则用分压表示的平衡常数KP=3/P
B.恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)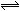 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、 2 mol和4 mol.若此时A、B和C均增加1 mol,平衡正向移动
2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、 2 mol和4 mol.若此时A、B和C均增加1 mol,平衡正向移动
C.恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)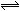 2NH3(g)达到平衡状态时,N2、H2、NH3各1 mol,若此时再充入3 mol N2,则平衡正向移动
2NH3(g)达到平衡状态时,N2、H2、NH3各1 mol,若此时再充入3 mol N2,则平衡正向移动
D.对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com