
| 实验目的 | 实验操作 | |
| A | 比较水和乙醇中氢的活泼性 | 分别讲少量钠投入到盛有水和乙醇的烧杯中 |
| B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和的FeCl3溶液中 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.钠与水反应比与乙醇反应剧烈;
B.水解生成HCl易挥发;
C.二者均与硝酸反应;
D.NaOH浓溶液滴加到饱和的FeCl3溶液,发生复分解反应生成沉淀.
解答 解:A.钠与水反应比与乙醇反应剧烈,则可比较水和乙醇中氢的活泼性,故A正确;
B.水解生成HCl易挥发,则蒸干不能制备MgCl2,故B错误;
C.二者均与硝酸反应,应选盐酸或稀硫酸反应后过滤,故C错误;
D.NaOH浓溶液滴加到饱和的FeCl3溶液,发生复分解反应生成沉淀,应在沸水中加饱和氯化铁制备胶体,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、盐类水解、混合物分离提纯、胶体制备为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.5 | B. | 1 | C. | 0.25 | D. | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氖元素的相对原子质量是a | |
| B. | 该氖原子的摩尔质量是aNAg | |
| C. | Wg该氖原子的物质的量一定是$\frac{W}{{a{N_A}}}$mol | |
| D. | Wg该氖气的体积是22.4$\frac{W}{{a{N_A}}}$升 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
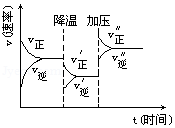 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | 正反应是吸热反应 | |
| B. | 若A、B是气体,则D是液体或固体 | |
| C. | 若A、B是气体,则C、D中至少有一种不是气体 | |
| D. | A、B、C、D均为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com