
Ζ÷Έω Θ®1Θ©ΔΌ≈®H2SO4ΒΡΈο÷ ΒΡΝΩ≈®Ε»c=$\frac{1000Π―ΠΊ}{M}$Θ§‘ΌΗυΨί»ή“ΚœΓ Ά«ΑΚσΈο÷ ΒΡΝΩ≤Μ±δΦΤΥψΥυ–η≈®ΝρΥαΒΡΧεΜΐΘΜ
ΔΎΗυΨί Β―ιΥυ–ηΒΡ≈®ΝρΥαΒΡΧεΜΐΘ§ΗυΨίΓΑ¥σΕχΫϋΓ±ΒΡ‘≠‘ρά¥―Γ‘ώΚœ ΒΡΝΩΆ≤ΘΜ
ΔέΗυΨί≈®ΝρΥαœΓ ΆΒΡΖΫΖ®Ζ÷ΈωΘΜ
Δή»ίΝΩΤΩ÷Μ”–“ΜΧθΩΧΕ»œΏΘ§÷ΜΡή≈δ÷Τ”κΤδΙφΗώΥυΕ‘”ΠΒΡΧεΜΐΒΡ»ή“ΚΘΜ
ΔίΗυΨίΕ®»ίΒΡ≤ΌΉςά¥Ζ÷ΈωΘΜ
Θ®2Θ©ΗυΨί≈δ÷Τ≤Ϋ÷η «ΦΤΥψΓΔ≥ΤΝΩΓΔ»ήΫβΓΔά以ΓΔ“Τ“ΚΓΔœ¥Β”ΓΔΕ®»ίΓΔ“Γ‘»ΓΔΉΑΤΩά¥Ζ÷ΈωΘΜ
Θ®3Θ©ΗυΨίc=$\frac{n}{V}$≤ΔΫαΚœ»ή÷ ΒΡΈο÷ ΒΡΝΩnΚΆ»ή“ΚΒΡΧεΜΐVΒΡ±δΜ·ά¥Ϋχ––Έσ≤νΖ÷ΈωΘ°
Ϋβ¥π ΫβΘΚΘ®1Θ©ΔΌ≈®H2SO4ΒΡΈο÷ ΒΡΝΩ≈®Ε»c=$\frac{1000ΓΝ1.84ΓΝ98%}{98}$mol/L=18.4mol/LΘ§
ΗυΨίœΓ ΆΕ®¬…Θ§œΓ Ά«ΑΚσ»ή÷ ΒΡΈο÷ ΒΡΝΩ≤Μ±δΘ§ά¥ΦΤΥψ≈®ΝρΥαΒΡΧεΜΐΘ§…η≈®ΝρΥαΒΡΧεΜΐΈΣxmLΘ§Υυ“‘xmLΓΝ18.4mol/L=500mLΓΝ0.5mol/LΘ§
ΫβΒΟΘΚxΓ÷13.6Θ§Υυ“‘”ΠΝΩ»ΓΒΡ≈®ΝρΥαΧεΜΐ «13.6mLΘ§
Ι ¥πΑΗΈΣΘΚ13.6mLΘΜ
ΔΎΗυΨίΓΑ¥σΕχΫϋΓ±ΒΡ‘≠‘ρΘ§Ι ”Π―Γ‘ώ20mLΒΡΝΩΆ≤Θ§Ι ¥πΑΗΈΣΘΚ20ΘΜ
Δέ≈®ΝρΥαœΓ ΆΒΡΖΫΖ®ΈΣΘΚœΓ Ά≈®ΝρΥα ±Θ§“ΣΑ―≈®ΝρΥαΜΚΜΚΒΊ―ΊΤς±ΎΉΔ»κ Δ”–Υ°ΒΡ…’±≠÷–Θ§Ά§ ±”Ο≤ΘΝßΑτ≤ΜΕœΫΝΑηΘ§“‘ Ι»»ΝΩΦΑ ±ΒΊά©…ΔΘ§Ζά÷Ι≈®ΝρΥαΖ…ΫΠΘΜ«–≤ΜΩ…Α―Υ°ΉΔ»κ≈®ΝρΥα÷–Θ§Ι ¥πΑΗΈΣΘΚΖά÷Ι≈®ΝρΥαΖ…ΫΠΘΜ
Δή»ίΝΩΤΩ÷Μ”–“ΜΧθΩΧΕ»œΏΘ§÷ΜΡή≈δ÷Τ”κΤδΙφΗώΥυΕ‘”ΠΒΡΧεΜΐΒΡ»ή“ΚΘ§Ι “Σ≈δ÷Τ500mL»ή“ΚΘ§‘ρ–κ―Γ‘ώ500mL»ίΝΩΤΩΘ§Ι ¥πΑΗΈΣΘΚ500mL»ίΝΩΤΩΘΜ
ΔίΕ®»ί ±Θ§“Σœ»Φ”Υ°÷ΝάκΩΧΕ»œΏ1-2cm¥ΠΘ§»ΜΚσ”ΟΫΚΆΖΒΈΙή÷πΒΈΦ”Υ°÷Ν“ΚΟφ”κΩΧΕ»œΏœύ«–Θ§Ι ¥πΑΗΈΣΘΚ1-2cmΘΜΫΚΆΖΒΈΙήΘΜ
Θ®2Θ©ΗυΨί≈δ÷Τ≤Ϋ÷η «ΦΤΥψΓΔ≥ΤΝΩΓΔ»ήΫβΓΔά以ΓΔ“Τ“ΚΓΔœ¥Β”ΓΔΕ®»ίΓΔ“Γ‘»ΓΔΉΑΤΩΩ…÷ΣΘ§”Π‘Ύ≈®ΝρΥαœΓ ΆΚσΫΪ»ή“Κά以÷Ν “Έ¬‘ΌΫχ––“Τ“ΚΒΡ≤ΌΉςΘ§
Ι ¥πΑΗΈΣΘΚΒΎΔή≤ΫΟΜ”–ΫΪœΓ ΆΚσΒΡ≈®ΝρΥαά以ΒΫ “Έ¬ΘΜ
Θ®3Θ©ΔΌ»τΫχ––≤ΌΉςΔίΕ®»ί ±Θ§―έΨΠΗ© ”Θ§‘ρΥυ≈δ÷Τ»ή“ΚΒΡΧεΜΐΫΪΤΪ–ΓΘ§‘ρ≈®Ε»ΫΪΤΪΗΏΘ§Ι ¥πΑΗΈΣΘΚΤΪΗΏΘΜ
ΔΎΈ ΧβΘ®2Θ©ΒΡ¥μΈσ «≤ΌΉςΫΪΟΜ”–ΫΪœΓ ΆΚσΒΡ≈®ΝρΥαά以ΒΫ “Έ¬Θ§‘ρά以Κσ»ή“ΚΧεΜΐΤΪ–ΓΘ§ΒΦ÷¬Υυ≈δ÷Τ»ή“ΚΒΡ≈®Ε»ΤΪΗΏΘ§Ι ¥πΑΗΈΣΘΚΤΪΗΏΘ°
ΒψΤά ±ΨΧβΩΦ≤ιΝΥ“ΜΕ®Έο÷ ΒΡΝΩ≈®Ε»»ή“ΚΒΡ≈δ÷ΤΙΐ≥Χ÷–ΒΡΦΤΥψΚΆΈσ≤νΖ÷ΈωΘ§ τ”ΎΜυ¥Γ–ΆΧβΡΩΘ§Ρ―Ε»≤Μ¥σΘ°


 ―τΙβ ‘ΨμΒΞ‘Σ≤β ‘ΨμœΒΝ–¥πΑΗ
―τΙβ ‘ΨμΒΞ‘Σ≤β ‘ΨμœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΕύ―ΓΧβ
| AΘ° | NaOHΘ®lΘ©+HClΘ®lΘ©®TNaClΘ®lΘ©+H2OΘ®lΘ© | BΘ° | Θ®NH4Θ©2CO3Θ®sΘ©®TNH4HCO3Θ®sΘ©+NH3Θ®gΘ© | ||
| CΘ° | 2COΘ®gΘ©+O2Θ®gΘ© $\frac{\underline{\;Βψ»Φ\;}}{\;}$2CO2Θ®gΘ© | DΘ° | CΘ®sΘ©+H2OΘ®gΘ© $\frac{\underline{\;ΗΏΈ¬\;}}{\;}$COΘ®gΘ©+H2Θ®gΘ© |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | NH4+ΓΔMg2+ | BΘ° | Mg2+ΓΔFe2+ | CΘ° | NH4+ΓΔFe2+ | DΘ° | Mg2+ΓΔAl3+ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | ΔΌΔΎ | BΘ° | ΔΌ | CΘ° | ΔΌΔέΔή | DΘ° | ΔΌΔί |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | Έο÷ ßΒγΉ”ΒΡΖ¥”ΠΈΣΜΙ‘≠Ζ¥”Π | |
| BΘ° | Έο÷ ‘Ύ±δΜ·÷– ß»ΞΒγΉ”Θ§¥ΥΈο÷ «―θΜ·ΦΝ | |
| CΘ° | ΖΔ…ζΒγΉ”ΉΣ“ΤΒΡΖ¥”ΠΦ¥ «―θΜ·ΜΙ‘≠Ζ¥”Π | |
| DΘ° | ΖΔ…ζΜ·ΚœΦέ…ΐΫΒΒΡΖ¥”Π≤Μ“ΜΕ® «―θΜ·ΜΙ‘≠Ζ¥”Π |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | 60ΘΚ36 | BΘ° | 36ΘΚ60 | CΘ° | 2ΘΚ1 | DΘ° | 1ΘΚ2 |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΧνΩ’Χβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | ΔΌΔΎΔί | BΘ° | ΔΌΔέΔό | CΘ° | ΔΎΔήΔί | DΘ° | ΔΌΔΎΔή |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
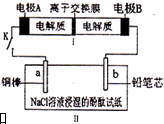 »γΆΦΥυ ΨΉΑ÷Ο «“Μ÷÷Ω…≥δΒγΒγ≥ΊΘ§ΉΑ÷ΟIIΈΣΒγΫβ≥ΊΘ°άκΉ”ΫΜΜΜΡΛ÷Μ‘ –μNa+Ά®ΙΐΘ§≥δΖ≈ΒγΒΡΜ·―ßΖΫ≥Χ ΫΈΣ2Na2S2+NaBr3$?_{≥δΒγ}^{Ζ≈Βγ}$Na2S4+3NaBrΘ°±’ΚœΩΣΙΊK ±Θ§bΦΪΗΫΫϋœ»±δΚλ…ΪΘ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
»γΆΦΥυ ΨΉΑ÷Ο «“Μ÷÷Ω…≥δΒγΒγ≥ΊΘ§ΉΑ÷ΟIIΈΣΒγΫβ≥ΊΘ°άκΉ”ΫΜΜΜΡΛ÷Μ‘ –μNa+Ά®ΙΐΘ§≥δΖ≈ΒγΒΡΜ·―ßΖΫ≥Χ ΫΈΣ2Na2S2+NaBr3$?_{≥δΒγ}^{Ζ≈Βγ}$Na2S4+3NaBrΘ°±’ΚœΩΣΙΊK ±Θ§bΦΪΗΫΫϋœ»±δΚλ…ΪΘ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©| AΘ° | ΗΚΦΪΖ¥”ΠΈΣ2S22--2e-=S42- | |
| BΘ° | Β±”–0.01 mol Na+Ά®ΙΐάκΉ”ΫΜΜΜΡΛ ±Θ§bΒγΦΪ…œΈω≥ωΤχΧε112 mL | |
| CΘ° | ±’ΚœKΚσΘ§bΒγΦΪΗΫΫϋΒΡpH±δ–Γ | |
| DΘ° | ±’ΚœKΚσΘ§aΒγΦΪ…œ”–ΤχΧε≤ζ…ζ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com