
【题目】用碳酸钠晶体(Na2CO310H2O),配制0.2mol/L的Na2CO3溶液480mL。
(1)所需主要仪器为:药匙、托盘天平、烧杯、玻璃棒、_________和胶头滴管。
(2)本实验所需称量碳酸钠晶体(Na2CO310H2O)_________g;
(3)根据下列操作对所配溶液的浓度产生的影响,完成下列要求。
①Na2CO310H2O晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有_________,偏低的有__________,无影响的有_________。(填序号)
(4)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:
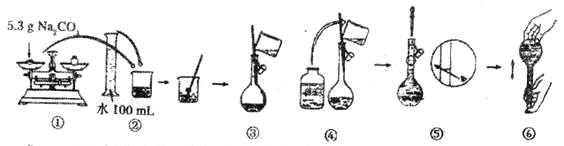
你认为该同学的操作步骤中错误(包含遗漏)之处有___________。
A.1处 | B.2处 | C.3处 | D.4处 |
【答案】(1)500mL容量瓶(无规格不得分)
(2)28.6
(3)①④ ②③ ⑤
(4)C(每空2分)
【解析】试题分析:(1)实验室没有480mL的容量瓶,配制时应该选用500mL的容量瓶,配制步骤有:计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以还缺少500 mL容量瓶,故答案为:500mL容量瓶;
(2)应用托盘天平称取Na2CO310H2O的晶体的质量为:m=nM=cVM=0.2mol/L×0.5L×286g/mol=28.6g,故答案为:28.6g;
(3)①碳酸钠失去了部分结晶水,导致称量溶质的质量增大,所以溶质的物质的量偏大,配制溶液的浓度偏高;②用“左码右物”的称量方法称量晶体导致称量溶质的质量增小,所以溶质的物质的量偏小,配制溶液的浓度偏低③碳酸钠晶体不纯,其中混有氯化钠,导致碳酸钠的物质的量偏小,配制溶液的浓度偏低;④称量碳酸钠晶体时所用砝码生锈,导致称量溶质的质量增大,所以溶质的物质的量偏大,配制溶液的浓度偏高;⑤容量瓶未经干燥就使用不影响溶质的物质的量,也不影响溶液的体积,所以对配制的溶液浓度无影响;故答案为:偏高的有①④,偏低的有②③,无影响的有⑤;
(4)①称量的固体的质量错误,所需要的Na2CO3质量为:m=nM=cVM=0.2mol/L×0.5L×106g/mol=10.6g,而不是5.3g;⑤定容时不应该仰视;⑥配制好后应该装入试剂瓶,贴上标签。故选C。


科目:高中化学 来源: 题型:
【题目】X、Y、Z 为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:
Y+X→甲(g),Y+Z→乙(g)。甲为10电子分子,Z为黄绿色气体。甲、乙可化合生成离子化合物。
(1)X 的电子式是______________。
(2)写出Y+X→甲(g)的化学方程式_____________________。
(3)向一定浓度的 BaCl2溶液中通入 SO2气体,未见沉淀生成,若在通入 SO2气体的同时加入或通入某纯净物(从X、Y、Z、甲、乙中选择),即可生成白色沉淀,该纯净物的化学式为________,生成的白色沉淀的化学式为___________。
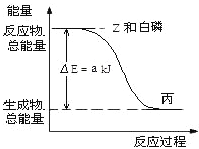
(4)已知常温下,PCl3为液体,PCl5为固体。白磷(P4)在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1 mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
已知1 mol白磷固体和Z气体反应,生成固态丁时,放热b kJ,则1 mol固态丁转化为液态丙时的反应热ΔH=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】γ-Fe2O3在磁性、催化、气敏等方面用途非常广泛,以硫铁矿烧渣(含Fe2O3、SiO2、CaO、Al2O3等)为原料生产γ-Fe2O3的流程如下:

(1)“还原焙烧”时,焦炭的作用是______________,起还原作用的主要物质是__________(填化学式)。
(2)“浸取”时,为提高铁的浸取率,可采取的措施除粉碎焙烧后的熔体、适当增大硫酸的用量外,还可采取的措施有______________(任写一条)。
(3)“过滤”前,将溶液的pH调至5~5.5的目的是将Al3+转化为___________(填化学式)。
(4)“缓慢干燥”生成铁黄的化学方程式为_____________。
(5)经上述流程制得的γ-Fe2O3中含有少量FeO和Al2O3杂质,某课题小组称取8.1380gγ-Fe2O3样品,溶于100mL2.00mol/LH2SO4溶液中,完全溶解后加入过量H2O2溶液,然后加入1.00mol/L的NaOH溶液,生成固体的质量与加入NaOH溶液体积的关系如图,则该样品中γ-Fe2O3的百分含量为___________(百分数保留到小数点后两位)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取浓度均为0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。将浓度均为0.1mol/L、体积均为1L的HA溶液和HB溶液分别加水稀释至体积为VL,溶液pH的变化曲线如图所示,则下列说法正确的是

A.HA是强酸,HB是弱酸
B.X是HB,Y是HA
C.常温下,pH相等的NaA溶液与NaB溶液的物质的量浓度:c(NaA)<c(NaB)
D.NaA与NaB的混合溶液中:c(Na+)+c(H+)=c(A-)+c(B-)+c(HA)+c(HB)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 乙烯、甲苯均能与溴水反应
B. 乙炔、苯均能与氢气反应
C. 苯酚、乙酸都能与氢氧化钠溶液反应
D. 乙醇、乙酸都能与钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器里,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知3v(B)=2v(A)、2v(C)=3v(B),则此反应可表示为
A. 2A+3B = 2C B. A+3B = 2C C. 3A+2B = 3C D. A+B = C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在该工艺中,理想状态是反应中原子全部转化为目标产物,即原子利用率为100%。利用以下各种化学反应类型的合成过程最符合绿色化学的是
A. 取代反应 B. 水解反应 C. 加聚反应 D. 酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学等多个领域潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是
3Fe2+2S2O![]() +O2+xOH-
+O2+xOH-![]() Fe3O4↓+S4O
Fe3O4↓+S4O![]() +2H2O。
+2H2O。
请回答下列问题:
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是__________________,S2O![]() 中S的化合价为________________.
中S的化合价为________________.
(2)反应的化学方程式中![]() =____________.
=____________.
(3)每生成 1mol Fe3O4,反应转移的电子为_________mol,被Fe2+还原的O2的物质的量为________mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上食用油的生产大多数采用浸出工艺。菜籽油的生产过程为:将菜籽压成薄片,用轻汽油浸泡,进行操作A;过滤,得液体混合物;对该混合物进行操作B,制成半成品油,再经过脱胶、脱色、脱臭即制成食用油。操作A和B的名称分别是
A.溶解、蒸发 B.萃取、蒸馏 C.分液、蒸馏 D.萃取、过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com