
|
工业合成氨的反应为 N2+3H2 | |
| [ ] | |
A. |
同时增大 |
B. |
同时减小 |
C. |
v1增大,v2减小 |
D. |
v1减小,v2增大 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| 高温高压 |
| ||
| 高温高压 |
| 化学键 | H-H | N≡N | H-N |
| 生成(或断裂)1mol化学键时放出(或吸收)的能量 | 436kJ | 946kJ | 390kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 一定条件 |
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市朝阳区高三上学期期末考试化学试卷(解析版) 题型:填空题
氨在国民经济中占有重要地位。
(1)工业合成氨时,合成塔中每产生1 mol NH3,放出46.1 kJ的热量。
① 工业合成氨的热化学方程式是 。
② 已知:
N2 (g) 2N
(g)
2N
(g)
H2 (g)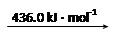 2H
(g)
2H
(g)
则断开1 mol N-H键所需的能量是_______kJ。
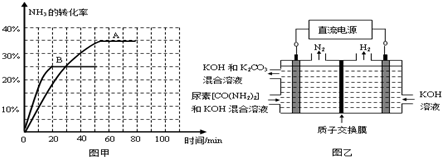
(2)下表是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。

① 曲线a对应的温度是 。
② 关于工业合成氨的反应,下列叙述正确的是 (填字母)。
A. 及时分离出NH3可以提高H2的平衡转化率
B. 加催化剂能加快反应速率且提高H2的平衡转化率
C. 上图中M、N、Q点平衡常数K的大小关系是K(M)= K(Q) >K(N)
③ M点对应的H2转化率是 。
 (3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
(3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g)。
则该燃料电池的负极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知::![]()
![]()
![]()
则![]() 的
的![]() =__________________________。
=__________________________。
(2)工业合成氮的反应为![]() 。在一定温度下,将一定量的N
。在一定温度下,将一定量的N![]() 和H
和H![]() 通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是___________________。
通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是___________________。
①增大压强 ②增大反应物的浓度
③使用催化荆 ④降低温度
(3) 工业合成氨的反应为![]() 。设在容积为2.0L的密闭容器中充入
。设在容积为2.0L的密闭容器中充入![]() 和
和![]() .反应在一定条件下达到平衡时,NH
.反应在一定条件下达到平衡时,NH![]() 的物质的量分数(NH
的物质的量分数(NH![]() 的物质的量与反应体系中总的物质的量之比)为
的物质的量与反应体系中总的物质的量之比)为![]() 。计算
。计算
①该条件下N![]() 的平衡转化率为______________;
的平衡转化率为______________;
②该条下反应![]() 的平衡常数为_____________。
的平衡常数为_____________。
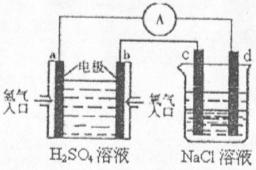
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行右图所示实验:(其中c、d均为碳棒。NaCI溶液的体积为500m1)
①a极为________极,电极反应式__________________________;
c极为________极,电极反应式__________________________
②右图装置中,当b极上消耗的O![]() 在标准状况下的体积为280ml时,则NaCl溶液
在标准状况下的体积为280ml时,则NaCl溶液
的PH为_________ (假设反应前后溶液体积不变,且NaCl溶液足量)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com