
将气体甲通入液体乙中得一混合液,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如下图所示,正确的是
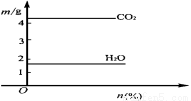
A.乙 烯 环己烷 B.甲烷 苯
烯 环己烷 B.甲烷 苯
C.乙炔 苯 D.乙烷 乙醇
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:选择题
已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,该条件下向100 mL的CaSO4饱和溶液中,加入400 mL 0.01 mol·L -1 的Na2SO4溶液,针对此过程的下列叙述正确的是(忽略混合过程中的体积变化)
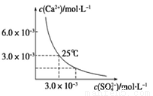
A.溶液中析出CaSO4沉淀,最终溶液中c(SO42-)较原来大
B.溶液中无沉淀析出,溶液中c(Ca2+ )、c(SO42-)都变小
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+ )、c(SO 42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO 42-)较原来大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
如下图表示4个碳原子相互结合的几种方式。小圆球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合,则下列说法正确的是 ( )
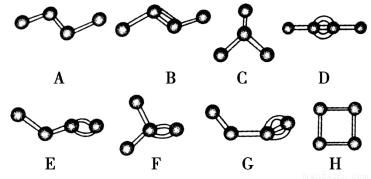
A.图中属于烷烃的是A、C、H
B.图中C和F分子中氢原子数相同
C.图中物质碳元素的质量分数最大的是C
D.图中与B互为同分异构体的有E、F、H
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期末化学试卷(解析版) 题型:选择题
某蓄电池反应式为:Fe+Ni2O3+3H2O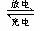 Fe(OH)2+2Ni(OH)2下列推断
Fe(OH)2+2Ni(OH)2下列推断 中正确的是
中正确的是
①放电时,Fe为正极,Ni2O3为负极;
②充电时,阴极上的电极反应式是:Fe(OH)2 +2e-=Fe+2OH-;
③充电时,Ni(OH)2为阳极;
④蓄电池的电极必须是浸在某碱性溶液中。
A.①②③ B.①②④ C.①③④ D.②③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期末化学试卷(解析版) 题型:选择题
下列说法或表示错误的是( )
A.等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量多
B.已知H2(g)+Cl2(g)===2HCl(g) ΔH=―184.6 kJ·mol-1,则有反应HCl(g)=== H2(g)+
H2(g)+ Cl2(g) ΔH=+92.3 kJ·mol-1
Cl2(g) ΔH=+92.3 kJ·mol-1
C.稀溶液中:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,则将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ
D.已知氧气较臭氧稳定,则3O2(g)===2O3(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期末化学试卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中进行如下可逆的反应:X(g)+Y(g) Z(g)+W(s);△H>0。下列叙述正确的是( )
Z(g)+W(s);△H>0。下列叙述正确的是( )
A.加入少量W,逆反应速率增大
B.因正反应吸热,所以升高温度正反应速率加快,逆反应速率减慢
C.当v(X)=v(Z)时,反应达到平衡
D.混合气体的密度不变时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一下期末化学试卷(解析版) 题型:填空题
(1)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出257.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为 。又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与过氧化氢反应生成液态水时放出的热量是 kJ。
(2)分别取40 mL 0.50 mol/L盐酸与 0.55 mol/L NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c = 4.18 J/(g·℃)。实验时,还需测量的数据有 。
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
某学生实验记录数据如下:

实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热为ΔH = ____________。
假定该学生的操作完全同上,实验中改用100 mL 0.50 mol/L盐酸跟100 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一下期末化学试卷(解析版) 题型:选择题
提高能源的利用率已成为国际能源研究的热点课题。下列相关措施使用不当的是( )
A.使燃料充分燃烧
B.加大能源开采力度
C.加强能源利用的科技投入
D.合理使用能源
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二下学期期末化学试卷(解析版) 题型:实验题
钠的化合物在工农业生产和人们的日常生活中有着广泛的应用,其中Na2O2常用作漂白剂和潜水艇中的供氧剂.Na2O2有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能反应.为了验证此推测结果,该同学设计并进行如下实验,实验步骤和现象如下:

步骤1:按如图组装仪器(图中夹持仪器省略)并检查装置的气密性,然后装入药品;
步骤2:打开K1、K2,产生的氢气在流经装有Na2O2的硬质玻璃管的过程中,没有观察到任何现象;
步骤3:检验完H2的纯度后,点燃酒精灯加热,观察到硬质玻璃管内Na2O2逐渐熔化,淡黄色的粉末慢慢变成了白色固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1.
根据以上信息回答下列问题:
(1)组装好仪器后,要检查装置的气密性.简述检查K2之前装置气密性的方法________;实验室利用A装置还可以制备的气体是________(写出1种即可).
(2)盛装CuSO4药品的仪器名称是________;B装置的作用是________;
(3)必须检验氢气纯度的原因是________;
(4)设置装置D的目的是________;
(5)由上述实验可推出Na2O2与H2反应的化学方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com