
【题目】如图所示,下列判断中正确的是
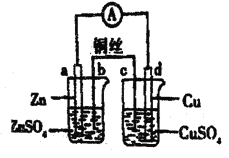
A. 电路中电子的流动方向为: adCuSO4(ag)cb
B. d电极反应式为: Cu2++2e-=Cu,反应后CuSO4溶液的浓度降低
C. C电极质量减少量等于d电极质量增加量
D. 该原电池原理为 Zn+ Cu2+= Zn2++Cu
【答案】C
【解析】A.电子从负极流向阴极,阳极流向正极,所以电子经外电路从a![]() d和c
d和c![]() b,电子不能通过电解质溶液,故A项错误;B. 该装置为原电池与电解池串联,左端装置为原电池,右端装置为电解池,a为负极,b为正极,c为阳极,d为阴极。由c为阳极,铜单质失电子被氧化为Cu2+,d为阴极,Cu2+得电子被还原为铜单质,二者得失电子守恒,所以d电极析出量与c电极溶解量相同,则硫酸铜的浓度不变,故B项错误;C项,由上述分析可知,c为阳极,铜单质失电子被氧化为Cu2+,d为阴极,Cu2+得电子被还原为铜单质,二者得失电子守恒,所以d电极析出量与c电极溶解量相同,故C项正确; D项,该装置为原电池与电解池串联,不是单独的原电池装置,故D项错误。综上所述,本题正确答案为C。
b,电子不能通过电解质溶液,故A项错误;B. 该装置为原电池与电解池串联,左端装置为原电池,右端装置为电解池,a为负极,b为正极,c为阳极,d为阴极。由c为阳极,铜单质失电子被氧化为Cu2+,d为阴极,Cu2+得电子被还原为铜单质,二者得失电子守恒,所以d电极析出量与c电极溶解量相同,则硫酸铜的浓度不变,故B项错误;C项,由上述分析可知,c为阳极,铜单质失电子被氧化为Cu2+,d为阴极,Cu2+得电子被还原为铜单质,二者得失电子守恒,所以d电极析出量与c电极溶解量相同,故C项正确; D项,该装置为原电池与电解池串联,不是单独的原电池装置,故D项错误。综上所述,本题正确答案为C。


科目:高中化学 来源: 题型:
【题目】一氧化碳、二氧化碳的利用具有十分重要的意义,科学家提出以下几个设想:
Ⅰ.二氧化碳与氢气在催化剂作用下可制取低碳烯烃。在一恒容密闭容器中分别投入1molCO2、3molH2,发生反应:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图所示。
C2H4(g)+4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图所示。
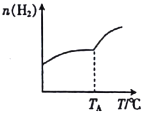
(1)其他条件不变,起始时若按1molCO2、2molH2进行投料,则CO2的转化率将____________(填“增大”“ 减小”或“不变”)。
(2)△H____________ (填“>”“<”或“不能确定”)0。
(3)若测试中体系内无氧气产生,试结合图示推断热稳定性:C2H4_______(填“>” “<”或“不能确定”)H2O。
Ⅱ.甲醇是重要的化工原料,又可作为燃料,工业上可利用CO或CO2来生产燃料甲醇。已知制备甲醇的有关反应的化学方程式以及在不同温度下的化学平衡常数如下表所示。
化学反应 |
| 500 | 700 | 800 |
①2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 1. 70 | 2.52 |
③3H2(g)+CO2 (g) | K3 |
请回答下列问题:
(4)根据反应比较△H1__________(填“>”“ <”或“不确定”)△H2。
(5)500℃时测得反应③在某时刻H2(g)、CO2
(6)下列措施能使反应③的平衡体系中![]() 增大的是___________(填字母)。
增大的是___________(填字母)。
A.将H2O(g)从体系中分离出去 B.充入He(g),使体系压强增大
C.升高温度 D.再充入1molH2
Ⅲ.(7)有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g),请你分析该设想能否实现?_______________(填“能”或“不能”),依据是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是部分矿物资源的利用及产品流程(如图),有关说法不平确的是
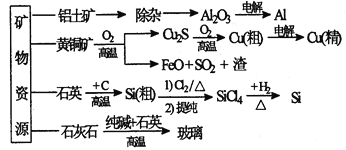
A. 粗铜电解精炼时,粗铜作阳极
B. 生产铝、铜、高纯硅及玻璃过程中都涉及氧化还原反应
C. 黄铜矿冶铜时,副产物SO2可用于生产硫酸,FeO可用作冶铁的原料
D. 粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题组以硫铁矿烧渣(含 Fe2O3、 Fe3O4、 Al2O3、 CaO、 SiO2 等)为原料制取软磁用 Fe2O3(要求纯度>99.2%, CaO 含量<0.01%)。其工艺流程如下(所加入试剂均稍过量):
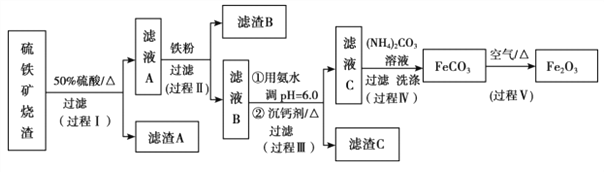
已知:生成氢氧化物的 pH 如下表所示
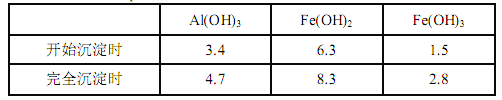
(1)滤渣 A 的主要成分是__________。
(2)在过程Ⅱ中可观察到产生少量气泡,溶液颜色慢慢变浅。能解释该实验现象的离子方程式有__________。
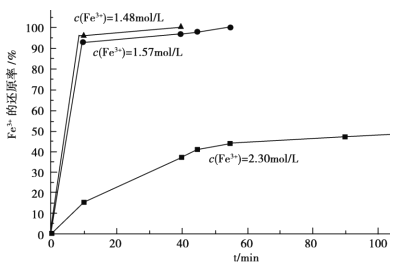
(3)在过程Ⅱ中,课题组对滤液 A 稀释不同倍数后,加入等质量的过量铁粉,得出 Fe3+浓度、还原率和反应时间的关系如图所示:结合上述实验结果说明:课题组选择稀释后c(Fe3+)为 1.60mol/L 左右的理由是______。
(4)在过程Ⅲ中,课题组在相同条件下,先选用了不同沉钙剂进行实验,实验数据见下表:(已知:滤液 B 中钙的含量以 CaO 计为 290—310mg/L)
沉钙剂 | Na2SO3 | H2C2O4 | (NH4)2CO3 | Na2CO3 | NH4F |
用量/g | 2 | 2 | 2 | 5 | 2 |
剩余CaO/mg/L) | 290 | 297 | 290 | 190 | 42 |
根据实验结果, 选择适宜的沉钙剂,得到滤渣 C 的主要成分有__________。
(5)在过程Ⅳ中,反应温度需要控制在 35℃以下,不宜过高,其可能的原因是__________。
(6)在过程Ⅴ中,反应的化学方程式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下实验操作正确的是
A.用量筒量取5.0 mL浓硫酸并直接在量筒中稀释
B.用嘴吹灭燃着的酒精灯火焰
C.称量NaOH固体时,将药品直接放在托盘上
D.给烧瓶里的液体加热时,垫上石棉网
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物中可能含有:K+、Na+、Clˉ、CO32—、SO42—等离子,将该固体溶解所得到的溶液进行如下实验:
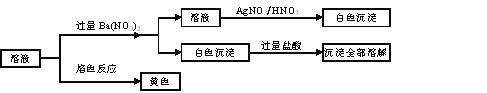
下列说法正确的是
A. 该混合物一定是Na2CO3和NaCl B. 该混合物可能是Na2CO3和KCl
C. 该混合物一定是K2CO3和NaCl D. 该混合物可能是Na2SO4和Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中,能大量共存的离子组是( )
A. K+、Cu2+、OH﹣、SO42- B. Fe3+、NH4+、NO3-、Cl﹣
C. K+、Na+、Cl﹣、CO32- D. K+、![]() 、MnO4-、SO42-
、MnO4-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 ______________。
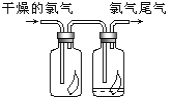
(2)为防止氯气尾气污染空气,可用________溶液吸收多余的氯气,原理是(用化学方程式表示)____________________。
(3)工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_______(用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com