
【题目】(1)某烃1mol与2molHCl完全加成,生成的氯代烷烃最多还可以与4mol氯气反应,则该烃的结构简式为__________________。
(2)某烷烃A蒸气的密度是相同状况下氢气密度的64倍,经测定得知A分子中共含6个甲基。若A不可能是烯烃与氢气加成的产物,A的结构简式为____________________;
(3)有下列五种烃: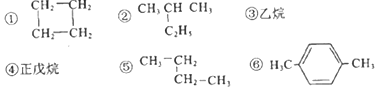
其中互为同分异构体的是_________________(填序号),②③④⑤四种物质按它们的沸点由低到高的顺序是________________(填序号),等质量的①③⑥三种物质,完全燃烧时消耗O2的物质的量由少到多的顺序为________________ 。
(4)按系统命名法,化合物(CH3)3CCH2CH(C2H5)CH3的名称是__________________。
3,5-二甲基-3-庚烯的结构简式是_____________________。
【答案】 CH![]() CH (CH3)3CCH2C(CH3)3 ② ④ ③⑤②④ ⑥①③ 2,2,4-三甲基己烷 CH3CH2C(CH3)=CHCH(CH3)CH2CH3
CH (CH3)3CCH2C(CH3)3 ② ④ ③⑤②④ ⑥①③ 2,2,4-三甲基己烷 CH3CH2C(CH3)=CHCH(CH3)CH2CH3
【解析】(1)烃![]() 与
与![]() 完全加成,生成的氯代烷最多还可以与
完全加成,生成的氯代烷最多还可以与![]() 反应,则A中含2个H,且存在碳碳三键,则烃的结构简式为CH
反应,则A中含2个H,且存在碳碳三键,则烃的结构简式为CH![]() CH ;正确答案: CH
CH ;正确答案: CH![]() CH。
CH。
(2)因气体的密度之比等于摩尔质量之比,烷烃A蒸气的摩尔质量为![]() ,则
,则![]() ,计算得出
,计算得出![]() ,所以烷烃A的分子式为
,所以烷烃A的分子式为![]() ,A不可能是氢气与烯烃加成的产物,说明A中两个C间不可能存在
,A不可能是氢气与烯烃加成的产物,说明A中两个C间不可能存在![]() 键,C只能构成4个键,因此得到A的结构简式: (CH3)3CCH2C(CH3)3;正确答案是: (CH3)3CCH2C(CH3)3 。
键,C只能构成4个键,因此得到A的结构简式: (CH3)3CCH2C(CH3)3;正确答案是: (CH3)3CCH2C(CH3)3 。
(3)①![]() 为环烷烃,与同碳原子数的烯烃属于同分异构体;②
为环烷烃,与同碳原子数的烯烃属于同分异构体;②![]() 为戊烷,属于饱和烷烃;③乙烷属于饱和烷烃;④戊烷为饱和烷烃;⑤
为戊烷,属于饱和烷烃;③乙烷属于饱和烷烃;④戊烷为饱和烷烃;⑤![]() 为丁烷,属于饱和烷烃;故②④分子式相同,结构不同,属于同分异构体;分子组成相似,相对分子质量越大,熔沸点越高,故②③④⑤四种物质按它们的沸点由低到高的顺序排列正确的是:③⑤②④,等质量的有机物燃烧时,含氢量越高,耗氧量越高,①③⑥三种物质,完全燃烧时消耗O2的物质的量由少到多的顺序为⑥①③,正确答案:② ④ ;③⑤②④; ⑥①③。
为丁烷,属于饱和烷烃;故②④分子式相同,结构不同,属于同分异构体;分子组成相似,相对分子质量越大,熔沸点越高,故②③④⑤四种物质按它们的沸点由低到高的顺序排列正确的是:③⑤②④,等质量的有机物燃烧时,含氢量越高,耗氧量越高,①③⑥三种物质,完全燃烧时消耗O2的物质的量由少到多的顺序为⑥①③,正确答案:② ④ ;③⑤②④; ⑥①③。
(4)烷烃命名时,选最长的碳链为主链,当有多条等长的碳链可选时,应选择支链多的为主链;从离支链近的一端给主链上的碳原子进行编号,当两端离支链一样近时,要从支链多的一端给主链编号;故该有机物主碳链为6个碳,为己烷;分子中在2号碳原子上有2个甲基,在4号碳原子上有1个甲基,因此化合物(CH3)3CCH2CH(C2H5)CH3的名称是2,2,4-三甲基己烷;主碳链为7个碳原子,在3、5号碳原子上各有1个甲基,碳碳双键在3位碳上,因此3,5-二甲基-3-庚烯的结构简式是CH3CH2C(CH3)=CHCH(CH3)CH2CH3;正确答案:2,2,4-三甲基己烷 ;CH3CH2C(CH3)=CHCH(CH3)CH2CH3。


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:
【题目】(题文)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

(1)反应Ⅰ:2H2SO4(l)![]() 2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)![]() SO2(g) ΔH3=-297 kJ·mol-1
SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:________________。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。

p2_______p 1(填“>”或“<”),得出该结论的理由是________________。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+![]() S↓+2I2+2H2O
S↓+2I2+2H2O
ii.I2+2H2O+_________![]() _________+_______+2 I-
_________+_______+2 I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则a=__________。
②比较A、B、C,可得出的结论是______________________。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物AM有如图所示转化关系,A与F分子中所含碳原子数相同,且均能与 NaHCO3溶液反应,F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色;D能发生银镜反应;M与NaOH溶液反应后的产物,其一氯代物只有一种。
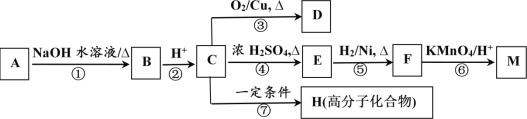
![]()
请回答:
(1)C、F的结构简式分别为___________________________、_______________________________。
(2)反应①⑦中,属于消去反应的是___________________(填反应序号)。
(3)反应③化学方程式为_____________________________________________________________;
反应⑦的化学方程式为_________________________________________________________。
(4)符合下列条件F的所有同分异构体的结构简式为_______________________________。
a.能发生银镜反应
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠广泛用于印染漂白、食品等行业,常作媒染剂、漂白剂、食品添加剂等。某兴趣小组用下列装證制备NaNO2。
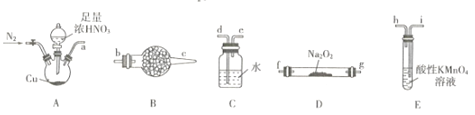
已知:①2NO+Na2O2=2NaNO2; ②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。
请回答下列问题:
(1)利用上图中的装置制备NaNO2,其连接顺序为a→__________(按气流方向,用小写字母表示)。
(2)实验开始时,先通一段时间N2的目的是__________。
(3)装置B中盛放试剂的名称为____,装置C的作用是_______。
(4)装置E中发生反应的离子方程式为_____________。
(5)为测定亚硝酸钠的含量,称取3.000g样品溶于水配成500mL.溶液,量取25.00mL溶液于锥形瓶中,硫酸酸化后加入过量KI,发生反应:2NO2-+2I-+4H+=2NO↑+I2+2H2O(杂质不参与反应)。然后用0.1000mol/LNa2S2O3标准溶液滴定至终点(发生反应:I2+2S2O32-=S4O62-+2I-),消耗20.00mL。
①该实验可选用的指示剂为_____,达到滴定终点时的现象是__________。
②所得样品中亚硝酸钠的质量分数为____________。
③下列操作会导致测定结果偏高的是_______(填代号)。
a.滴定过程中向锥形瓶中加少量水
b.消定前滴定管尖嘴部分有气泡,滴定后气泡消失
c.读数时,滴定前仰视,滴定后府视
d.滴定时,标准被滴到锥形瓶外
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol NaOH的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·L-1
mol·L-1
C. (2b-a) mol·L-1 D. (10b-5a) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法错误的是( )
A. 1 L 0.1 mol·L-1 NaF溶液中含有0.1NA个F-
B. 32 g硫跟足量金属铜反应转移电子数为2NA
C. 48 g O2和O3的混合气体中含有3NA个氧原子
D. 1 mol H2O中含有2NA个共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为探究H2O2、H2SO3、Br2的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
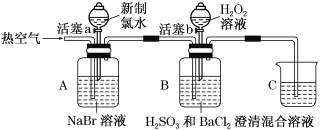
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加少量新制氯水,关闭活塞a | A中溶液变为浅红棕色 |
Ⅱ | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | B中开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)实验操作Ⅰ时,A中反应的离子方程式为__________________________。
(2)实验操作Ⅱ吹入热空气的目的是________________________________。
(3)装置C的作用是______________________;C中盛放的药品是________。
(4)实验操作Ⅲ中混合液逐渐变成红棕色,其对应的离子方程式为_____________。
(5)由上述实验得出的结论是______________________________________。
(6)①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否有干扰,理由是_______________________________________________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是________________(写出一条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:3A(g)![]() 3B(?)+C(?)△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是( )
3B(?)+C(?)△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是( )
A. B和C可能都是固体 B. 若C为固体,则B一定是气体
C. B和C一定都是气体 D. B和C不可能都是气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com