
| A. | 金属钠 | B. | 溴水 | C. | 碳酸钠溶液 | D. | 酚酞试剂 |
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:填空题
粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.15 L 6.0 mol·L-1盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12 L(标况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填空:
(1) ①中引发铝热反应的实验操作是_____________,产物中的单质B是_____________。
①中引发铝热反应的实验操作是_____________,产物中的单质B是_____________。
(2)②中所发生的各反应的化学方程式是_______________________。
(3)③中所发生的各反应的离子方程式是_________________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为__________,c(Fe2+)为__________。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
元素X的单质及X与Y形成的化合物能按如下图所示的关系发生转化(其中m≠n,且均为正整数)。下列说法正确的是
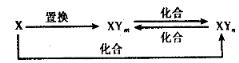
A.X一定为非金属元素 B.X、Y可能均为非金属元素
C.若X为Fe,Y可为Cl、Br和I D.若X为Fe,Y只能为Cl
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 或
或 .
.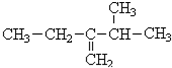 2-乙基-3-甲基-1-丁烯;
2-乙基-3-甲基-1-丁烯;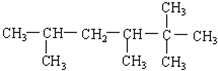 2,2,3,5-四甲基己烷.
2,2,3,5-四甲基己烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部由非金属元素组成的化合物一定是共价化合物 | |
| B. | 含有共价键的化合物不一定是共价化合物 | |
| C. | 由共价键形成的分子一定是共价化合物 | |
| D. | 硫酸分子中有H+和SO42-两种离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验所用试剂或操作 | 实 验 现 象 | 验证的性质 |
| 碘化钾淀粉溶液 | ||
| 取适量过氧化氢溶液于试管中,加热,用带火星的木条检验. |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
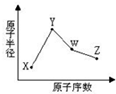 X、Y、W、Z是四种常见的短周期元素,其原子半径随原子序数表化如下图所示.已知X的一种核素的质量数为18,中子数为10,Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.
X、Y、W、Z是四种常见的短周期元素,其原子半径随原子序数表化如下图所示.已知X的一种核素的质量数为18,中子数为10,Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.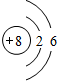 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和稀HNO3反应后的溶液pH=1:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | 碳酸氢镁溶液中加入过量澄清石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓ | |
| C. | 0.01 mol/L NH4Al(SO4)2溶液与0.02 mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 碳酸氢钠溶液与过量的澄清石灰水反应:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com