

| 1 |
| 2 |
| 1 |
| 2 |
| 0.3 |
| 20 |
| c(N 2O 4) |
| c 2(NO2) |
| 0.6mol/L |
| (0.3mol/L) 2 |
| c(N 2O 4) |
| c 2(NO2) |
| 0.6mol/L |
| (0.3mol/L) 2 |


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
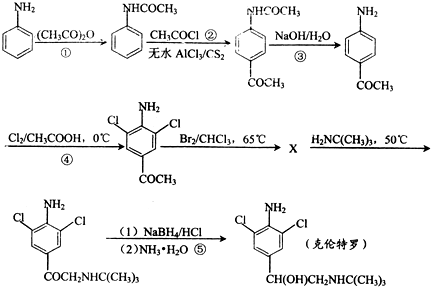
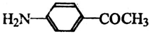 ) 的同分异构体有多种,请写出符合以下条件的其中任意一种
) 的同分异构体有多种,请写出符合以下条件的其中任意一种查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若盐酸的浓度为0.2mol/L,则第一次测出的盐酸的浓度偏高 |
| B、若NaOH中混有少量的Na2CO3,则测定的结果偏高 |
| C、开始读数时仰视滴定管读数,滴定结束时也仰视滴定管读数,对实验结果无影响 |
| D、第二次测定的数据可能是由于滴定时不小心把盐酸滴到锥形瓶外面引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用激光笔光束鉴别氯化铁溶液和氢氧化铁胶体 |
| B、用KSCN溶液鉴别Fe3+和Fe2+ |
| C、用氨水鉴别Al3+和Mg2+ |
| D、用焰色反应鉴别碳酸钠溶液和碳酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.12 g |
| B、2.2 g |
| C、3.2g |
| D、6.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe和Cl2 |
| B、NaOH和SO2 |
| C、Na和O2 |
| D、C和O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com