
|
将20 mL 0.5 mol/L Al2(SO4)3溶液加水稀释到500 mL,稀释后溶液中SO42-浓度为 | |
| [ ] | |
A. |
0.01 mol/L |
B. |
0.02 mol/L |
C. |
0.03 mol/L |
D. |
0.06 mol/L |
科目:高中化学 来源:山东省日照一中2011-2012学年高一上学期期中考试化学试题 题型:013
|
下列有关Fe(OH)3胶体的制备方法正确的是 | |
| [ ] | |
A. |
将1~2 ml饱和FeCl3溶液逐滴滴到20 ml 0.5 mol·L-1 NaOH溶液中 |
B. |
将1~2 ml饱和FeCl3溶液逐滴加入到20 ml沸水中,并继续加热至溶液呈红褐色后停止加热 |
C. |
将1~2 ml饱和FeCl3溶液逐滴加入到20 ml冷水中,再加热至沸腾 |
D. |
将1~2 ml沸水加入到1~2 ml FeCl3饱和溶液中,并用玻璃棒不断搅拌 |
查看答案和解析>>
科目:高中化学 来源:山东省巨野一中2010-2011学年高二“每周一练”化学试题 题型:022
医学上在进行胃肠疾病的检查时,利用X射线对BaSO4穿透能力较差的特性,常用BaSO4做内服造影剂,这种检查手段称为钡餐透视.
Ⅰ.请写出BaSO4能作为钡餐透视的另外一个理由:________.
Ⅱ.请用文字叙述和离子方程式说明钡餐透视时为什么不用BaCO3?________.
Ⅲ.某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:
①5 mL水
②20 mL 0.5 mol·L-1的Na2SO4溶液
③40 mL 0.2 mol·L-1的Ba(OH)2溶液
④40 mL 0.1 mol·L-1的H2SO4溶液中,溶解至饱和.
(1)以上各溶液中,c(Ba2+)的大小顺序正确的是________,BaSO4的溶解度的大小顺序为________(填序号).
A.③>①>④>②
B.③>①>②>④
C.①>④>③>②
D.①>③>④>②
(2)已知25℃时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液③中的c(SO![]() )为________,溶液②中c(Ba2+)为________.
)为________,溶液②中c(Ba2+)为________.
(3)某同学取同样的溶液③和溶液④直接混合,则混合溶液的pH为________(假设混合后溶液的体积为混合前两溶液的体积之和).
查看答案和解析>>
科目:高中化学 来源:黑龙江省哈六中2012届高三上学期期末考试化学试题 题型:022
A、B、C三种短周期元素在周期表中相对位置如图:
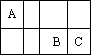
(1)A与C形成的液态化合物是常见的重要有机溶剂,则A、B、C三种元素最高价氧化物对应的水化物酸性由强到弱的顺序是:________>________>________(用化学式表示).
(2)X、Y为B、C两种元素形成的单质,标准状况下,X的密度为3.17 g·L-1.Z是一种化合物,焰色反应呈紫色(透过蓝色钴玻璃),室温下0.1 mol·L-1 Z水溶液pH=13.X、Y、Z有如图转化关系:
①写出X与Z反应的离子方程式:________.
②已知丙能与稀硫酸反应生成能使品红褪色的气体.丁的化学式为________,丁的水溶液pH>7的原因是:________(用离子方程式表示).
③将20 mL 0.5 mol/L丙溶液逐滴加入20 mL 0.2 mol/L KMnO4溶液(硫酸酸化)中,恰好褪色.写出反应的离子方程式________.
查看答案和解析>>
科目:高中化学 来源:湖北省襄阳五中2012届高三上学期期中考试化学试题 题型:022
有A、B、C、D四种短周期元素在周期表中相对位置如下图:
(1)A与D形成的液态化合物是常见的重要有机溶剂,
则A、B、C、D四种元素最高价氧化物对应的水化物酸
性由强到弱的顺序是:________>________>________>________(用化学式表示),B、C、D三种元素的第一电离能由大到小的顺序是:________(用元素符号表示)
(2)X、Y为C、D两种元素形成的单质.标准状况下,X的密度为3.17 g/L.Z是一种化合物,焰色反应呈紫色(透过蓝色钴玻璃),室温下0.1 mol/L Z水溶液pH=13.X、Y、Z有如图转化关系:
①写出X与Z反应的离子方程式:________
②已知丙能与稀硫酸反应生成使品红褪色的气体.丁的化学式________,丁的水溶液pH>7的原因:________(用离子方程式表示)
③将20 mL 0.5 mol/L丙溶液逐滴加入20 mL 0.2 mol/L KMnO4溶液(硫酸酸化)中,恰好褪色.写出反应的离子方程式________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com