
 A��g��+3B��g��?2C��g����Ӧ���ܱ������н��У��������ݻ����䣬���¶ȷֱ�ΪT1��T2ʱ���ﵽƽ�⣬B�����������ʱ��Ĺ�ϵ��ͼ��ʾ������һ����ɱ���ܱ�������ͨ������ʵ�����A�����B���壬�ں��������·�����Ӧ����ƽ��״̬����������¶ȣ�������Ӧһ��ʱ���ﵽƽ��״̬��������������ȷ���ǣ�������
A��g��+3B��g��?2C��g����Ӧ���ܱ������н��У��������ݻ����䣬���¶ȷֱ�ΪT1��T2ʱ���ﵽƽ�⣬B�����������ʱ��Ĺ�ϵ��ͼ��ʾ������һ����ɱ���ܱ�������ͨ������ʵ�����A�����B���壬�ں��������·�����Ӧ����ƽ��״̬����������¶ȣ�������Ӧһ��ʱ���ﵽƽ��״̬��������������ȷ���ǣ�������| A�� | T1��T2���÷�Ӧ����������������ڷ�Ӧ��������� | |
| B�� | �÷�Ӧ�ڸ���ʱ�����Է����� | |
| C�� | ��ƽ��״̬��ƽ��״̬��Ĺ����У�ƽ���������ƶ���A���������һֱû�б仯 | |
| D�� | ��ӳ�ӿ�ʼ��ƽ��״̬��Ĺ����У�ƽ�ⳣ��K��A��ת���ʶ�����������С |
���� A����ͼ���ȹ���ֵ��֪T1��T2�������¶�B�������������˵�������¶�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ��
B�����ڸ������Է����У��������G=��H-T•��S��0��
C����������ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�������ƶ��жϣ�
D������ƽ�ⳣ��ֻ���¶��йأ���Ũ���أ�ƽ��������У���Ӧ��ת����������֮����Ӧ��ת���ʼ��٣�
��� �⣺A����ͼ���ȹ���ֵ��֪T1��T2�������¶�B�������������˵�������¶�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ�����Է�Ӧ����������������ڷ�Ӧ�������������A����
B����Ӧ�ġ�H��0����S��0���ڵ����¡�G=��H-T•��S��0����Ӧ���Է����У���B����
C��������ʵ�����A�����B����Ϊnmol����Ӧ��AΪamol����
A+3B 2C��
2C��
��ʼ��mol�� n n 0
��Ӧ��mol�� a 3a 2a
����ʱ�̣�mol��n-a n-3a 2a
��ʼʱA���������Ϊ$\frac{n}{n+n}$100%=50%������ʱ��A���������Ϊ$\frac{n-a}{n-a+n-3a+2a}$��100%=50%��A���������һֱû�б仯����C��ȷ��
D����Ӧ�ӿ�ʼ��ƽ��״̬��Ĺ����У���Ӧ������ƽ�⣬Ȼ�����£�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ��K���Dz���Ȼ���С��A��ת���������������٣���D����
��ѡC��
���� ���⿼�黯ѧƽ��ͼ�����⣬��Ŀ�ѶȽϴ�ƽ�����η������֪�����۷�Ӧ��ν���A���������һֱû�б仯�ǽ�����ѵ㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ع���ʱ��пʧȥ���� | |
| B�� | ��ع���ʱ������������ͨ�����·���� | |
| C�� | ��������ĵ缫��ӦʽΪ��2MnO2+H2O+2e-�TMn2O3+2OH- | |
| D�� | ���·��ÿͨ��0.2 mol���ӣ�п�����������ϼ�С6.5 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
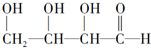 ��
��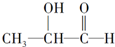
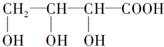 ��
��
| A�� | �ڢ� | B�� | �٢� | C�� | �ۢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��A��B��C��D��E��F�������ʣ����ǵ��ת����ϵ��ͼ����Ӧ���������ֲ������ԣ�����֪A��B��E��Ϊ���ʣ�B��E�ڳ�����Ϊ���壬CΪ����ɫ���壮�ش��������⣺
��A��B��C��D��E��F�������ʣ����ǵ��ת����ϵ��ͼ����Ӧ���������ֲ������ԣ�����֪A��B��E��Ϊ���ʣ�B��E�ڳ�����Ϊ���壬CΪ����ɫ���壮�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
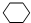 �������ǻ����飮
�������ǻ����飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ͼ1װ������Cu��ŨH2SO4��Ӧ��ȡ������SO2���� | |
| B�� | ͼ2װ�����ڷ���ˮ���屽�Ļ���� | |
| C�� | ͼ3װ�������Ʊ����ռ�NO���� | |
| D�� | ͼ4װ�����ڳ�ȥ̼�����ƹ����е�����̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȼ��ʱ�ǵ���ɫ�����Ļ��� | B�� | ��ʹ��ˮ��ɫ | ||
| C�� | ����H2�����ӳɷ�Ӧ | D�� | ����HCl�ӳ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com