
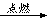 C
C 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:不详 题型:实验题
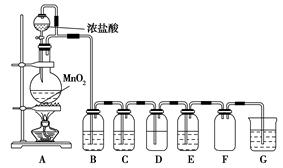
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
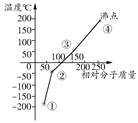
| A.单质①是最活泼的非金属单质 |
| B.单质②能使品红溶液褪色 |
| C.单质③在常温下是液态 |
| D.单质的氧化性强弱顺序是④>③>②>① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硅材料广泛应用光纤通讯 |
| B.工艺师利用盐酸刻蚀石英制作艺术品 |
| C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D.粗硅制备单晶硅不涉及氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2 | B.Br2 | C.HCl | D.CO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.闻Cl2气味 | B.除去Cl2中的HCl |
| C.干燥Cl2 | D.用高锰酸钾和浓盐酸快速制取Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
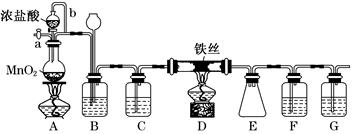
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 |
| B.同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等 |
| C.将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成 |
| D.将足量Cl2通入NaBr、NaI的混合溶液中,反应后将溶液蒸干并充分灼烧,剩余的固体物质成分为NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com