
 NaClO具有强氧化性,其溶液可用于游泳池及环境消毒.
NaClO具有强氧化性,其溶液可用于游泳池及环境消毒.| 1mol |
| 2mol |


科目:高中化学 来源: 题型:
| C% | H% | O% |
| 40.00% | 6.67% | 53.33% |
查看答案和解析>>
科目:高中化学 来源: 题型:
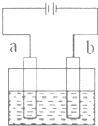
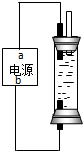
| A、b电极上发生氧化反应 |
| B、该装置能将化学能转变成电能 |
| C、电解质溶液中Cl-向a电极迁移 |
| D、若b为铁,则b电极的反应式为:Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
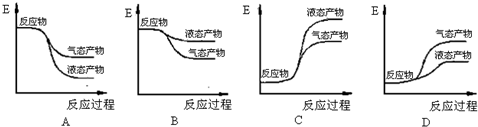
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、t℃时,50g甲的饱和溶液中溶解了10g的甲 |
| B、将t2℃甲、乙两种物质的饱和溶液升温至t3℃(溶剂的量不变),两种溶液中溶质的质量分数相等 |
| C、t2℃时,要使接近饱和的乙溶液达到饱和状态,可采用蒸发溶剂的方法 |
| D、分别将t2℃甲、乙两种物质的溶液降温至t1℃,一定都有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定不含K+ |
| C、将某气体通入溴水中,溴水颜色褪去,该气体一定是SO2 |
| D、向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2可用于制备光导纤维 |
| B、MgO和Al2O3均只能与酸反应,不能与碱反应 |
| C、液氯就是氯气的水溶液,它能使干燥的有色布条褪色 |
| D、Mg和Fe在一定条件下与水反应都生成H2和对应的碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com