
已知某反应A(g)+B(g)??C(g)+D(g)过程中的能量变化如图所示,回答问题。

该反应是 (填“吸热”或“放热”)反应,该反应的ΔH= kJ/mol(用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量 (填“一定高”“一定低”或“高低不一定”)。
科目:高中化学 来源:2014年高中化学人教版选修四第四章 电化学基础练习卷(解析版) 题型:填空题
如图所示,p、q为直流电源的两极,A由金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D上产生气泡,试回答:

(1)p为 极,A极发生了 反应。
(2)C为 极,可收集到 ;D为 极,可收集到 。
(3)C极的电极反应式为 。
(4)在电解过程中,测C、D两极上产生气体的体积,实验数据如下表:
时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
阴极产生气体 的体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
阳极产生气体 的体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
仔细分析以上实验数据,请说出变化的可能原因是
。
(5)当反应进行一段时间后,A、B电极附近溶液的pH (填“增大”“减小”或“不变”)。
(6)当电路中通过0.004 mol电子时,B极上沉积的金属X为0.128 g,则此金属的摩尔质量为 。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第二章 化学反应速率与化学平衡练习卷(解析版) 题型:选择题
对于某一可逆反应,在不同条件下的平衡状态中,正、逆反应速率的关系是( )

查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第三章 水溶液中的离子平衡练习卷(解析版) 题型:选择题
下列水溶液一定呈中性的是( )
A.c(NH4+)=c(Cl-)的NH4Cl溶液
B.c(H+)=1.0×10-7 mol·L-1的溶液
C.pH=7的溶液
D.室温下将pH=3的酸与pH=11的碱等体积混合后的溶液
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第三章 水溶液中的离子平衡练习卷(解析版) 题型:选择题
能使水的电离平衡右移,且水溶液显碱性的离子是( )
A.H+ B.OH- C.Al3+ D.HCO3-
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第一章 化学反应与能量练习卷(解析版) 题型:选择题
含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6 kJ。下列热化学方程式中正确的是( )
A.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=+114.6 kJ/mol
B.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=-114.6 kJ/mol
C. Ba(OH)2(aq)+HCl(aq)=
Ba(OH)2(aq)+HCl(aq)=  BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol
BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol
D.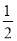 Ba(OH)2(aq)+HCl(aq)=
Ba(OH)2(aq)+HCl(aq)=  BaCl2(aq)+H2O(l) ΔH=+57.3 kJ/mol
BaCl2(aq)+H2O(l) ΔH=+57.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第一章 化学反应与能量练习卷(解析版) 题型:选择题
实验室进行中和热测定的实验时除需要大烧杯(500 mL)、小烧杯(100 mL)外,所用的其他仪器和试剂均正确的一组是( )
A.0.50 mol·L-1盐酸,0.50 mol·L-1NaOH溶液,100 mL量筒1个
B.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,100 mL量筒2个
C.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒1个
D.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒2个
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四模块质量检测练习卷(解析版) 题型:选择题
实验测得常温下0.1 mol/L某一元酸(HA)溶液的pH不等于1,0.1 mol/L某一元碱(BOH)溶液里: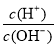 =10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
=10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
A.c(B+)>c(A-)>c(OH-)>c(H+)
B.c(A-)>c(B+)>c(H+)>c(OH-)
C.c(H+)>c(A-)>c(OH-)>c(B+)
D.c(B+)>c(A-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014年7月山东省泰安市高二年级考试化学(物质结构与性质)试卷(解析版) 题型:填空题
(8分)已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子对数与未成对电子数之比为3:1。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1∶1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
(1)D元素在元素周期表中的位置为第 周期 族。
(2)下列叙述正确的是 (填写序号)。
a.水的沸点比M高得多,是因为水分子间能形成氢键,而M分子间不能形成氢键
b.M的中心原子采用sp3杂化
c.N分子中含有6个σ键和1个大π键
d.BD2晶体的熔点、沸点都比二氧化硅晶体的低
(3)已知C2D是一种麻醉剂,根据等电子原理可推知C2D的空间构型为 。
(4)E的一种氧化物Q,其晶胞结构如图所示,则Q的化学式为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com