
| A. | 其他条件不变,增大压强,平衡不发生移动 | |
| B. | 其他条件不变,增大压强,混合气体的总质量不变 | |
| C. | 该反应式中n值一定为2 | |
| D. | 原混合气体中A与B的物质的量之比为2:1,且2M(A)+M(B)=3M(D)(其中M表示物质的摩尔质量) |
分析 A.增大压强平衡向气体体积减小的分析移动;
B.增大压强平衡向正反应方向移动,根据质量守恒定律判断混合气体的质量变化;
C.C为固体,压强改变不影响C的浓度,不能确定n的值;
D.原混合气中A与B的物质的量之比为2:1,按2:1反应,混合气体中二者始终为2:1,二者的平均相对分子质量与D的相对分子质量相等,则混合气体的平均相对分子质量为定值.
解答 解:A.该反应正反应是气体体积减小的反应,增大压强平衡向正反应方向移动,故A错误;
B.增大压强平衡向正反应方向移动,C的质量增大,C为固体,根据质量守恒定律可知,混合气体的质量减小,故B错误;
C.C为固体,压强改变不影响C的浓度,不能确定n的值,故C错误;
D.增大压强,测得混合气体的平均相对分子质量不变,说明混合气体的平均相对分子质量为定值,原混合气中A与B的物质的量之比为2:1,按2:1反应,混合气体中二者始终为2:1,二者的平均相对分子质量与D的相对分子质量相等,则混合气体的平均相对分子质量为定值,故2M(A)+M(B)=3M(D),故D正确,
故选D.
点评 本题考查化学平衡的影响因素,难度不大,D选项关键是判断混合气体的平均相对分子质量为定值.


科目:高中化学 来源: 题型:选择题
| A. | 化合物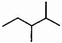 按系统命名法的名称为2,3一二甲基丁烷 按系统命名法的名称为2,3一二甲基丁烷 | |
| B. | 淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体 | |
| C. | 等质量的聚乙烯、甲烷、乙烯分别充分燃烧,所耗氧气的量依次减少 | |
| D. | 通常用酒精消毒,其原理是酒精使细菌中的蛋白质变性而失去生理活性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
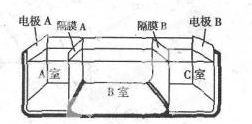 水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铁可用作净水剂 | B. | 二氧化硅可用作计算机芯片 | ||
| C. | 铜制容器可用于盛装浓硝酸 | D. | 醋酸铅可用于分离提纯蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 双氧水是一种对环境友好的消毒剂、漂白剂,广泛应用于化工、医药、环保等领域.请回答下列问题:
双氧水是一种对环境友好的消毒剂、漂白剂,广泛应用于化工、医药、环保等领域.请回答下列问题: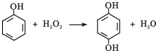 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 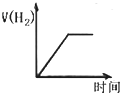 | B. | 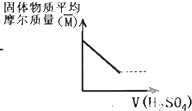 | ||
| C. | 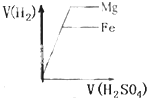 | D. | 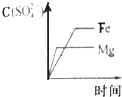 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某无色溶液中:NH4+、Na+、Cl-、MnO4- | |
| B. | 常温下由水电离出的c(H+)=1×10-13mol•L-1的溶液中:Na+、K+、SO32-、CO32- | |
| C. | 在c(H+)=1×10-13mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH=1的溶液中:K+、Mg2+ SiO32- SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,14 g C2H4、C3H6的混合气体中含有碳原子的数目为NA | |
| B. | 常温下,pH=12的Na2CO3溶液中含有的OH-离子数为0.01NA | |
| C. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.2 NA | |
| D. | 7.8 g Na2O2中含有的阴离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物的转化率 | B. | 反应体系的压强 | ||
| C. | 正、逆反应的速率 | D. | 反应混合物的浓度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com