


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.二氧化硅可用作半导体材料 | B.硝酸常用作金属铜加工前的酸洗 |
| C.碳酸钠可用于治疗胃酸过多 | D.三氧化二铁常用于生产红色油漆和涂料 |
查看答案和解析>>
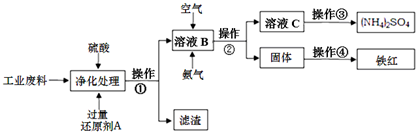
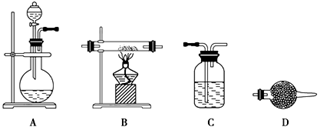
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
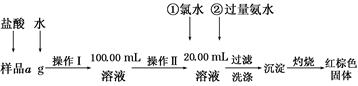
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
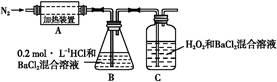
科目:高中化学 来源:不详 题型:实验题
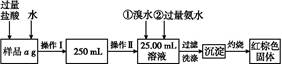
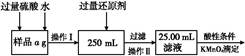
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
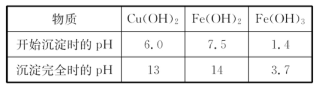

| A.氯水 | B.H2O2 | C.NaOH | D.CuO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
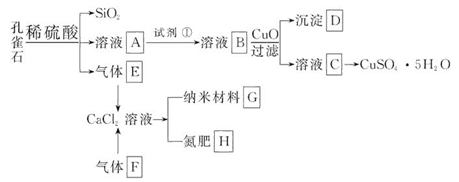
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2+的水溶液为浅绿色 |
| B.Fe3+的水溶液为黄色 |
| C.Fe3+具有氧化性,Fe2+具有还原性 |
| D.Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com