
判断下列有关化学基本概念的依据正确的是
A.溶液与胶体:本质不同的原因是能否发生丁达尔效应
B.共价化合物:是否含有共价键
C.强弱电解质:溶液的导电能力大小
D.氧化还原反应:元素是否发生电子转移
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届山东省邹城市高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24 L CCl4中含Cl原子数目为0.4NA
B.白磷分子(P4)呈正四面体结构,12.4 g白磷中含有P-P键数目为0.6NA
C.1mol氯气参加氧化还原反应,转移的电子数一定为2 NA
D.5.6g Fe和足量的盐酸反应时,失去的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第二次模拟测试化学试卷(解析版) 题型:选择题
下列离子方程式表示正确的是
A.AgNO3 溶液中加入Cu :Cu+Ag+=Cu2++Ag
B.NaHCO3溶液中加入CH3COOH: CO32-+2CH3COOH=CO2↑+2CH3COO-+H2O
C.含0.2mol FeBr2 的溶液中通入0.2mol Cl2 :
4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl-
D.等体积等物质的量浓度的NaHCO3和Ba(OH)2溶液混合:
HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2016届浙江省瑞安市四校高三上学期第一次联考化学试卷(解析版) 题型:选择题
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是
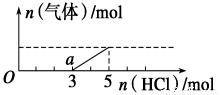
A.O点溶液中所含溶质的化学式为NaOH、Na2CO3
B.常温下,a点溶液pH>7
C.标准状况下,通入CO2的体积为4.48L
D.原NaOH溶液的物质的量浓度为2.5mol/L
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁均有水珠 | 两种物质均受热分解 |
B | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
C | 向NaBr溶液中滴入少量氯水和苯,振荡、静置 | 溶液上层呈橙红色 | Br—还原性强于Cl— |
D | 向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第三次模拟化学试卷(解析版) 题型:选择题
如图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是
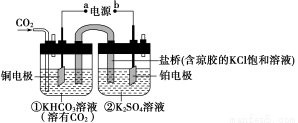
A.该过程是电能转化为化学能的过程
B.一段时间后,①池中n(KHCO3)不变
C.一段时间后,②池中溶液的pH一定下降
D.铜电极的电极反应式为CO2+8H++8e-===CH4+2H2O
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:选择题
下列各组离子在溶液中能够大量共存,当溶液中c(H+)=10-1 mol·L-1时有气体产生;而当溶液中c(H+)=10-13 mol·L-1时又能生成沉淀。则该组离子可能是
A.Na+、Ba2+、NO3―、CO32―
B.Fe2+、Na+、SO42―、NO3―
C.Mg2+、NH4+、SO42-、Cl-
D.Ba2+、K+、Cl-、NO3―
查看答案和解析>>
科目:高中化学 来源:2016届安徽省三校高三上学期二次模拟化学试卷(解析版) 题型:填空题
(6分)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO的浓度,某兴趣小组提出以下两种方案:
a.在微碱性条件下,用Fe(OH)2还原NO3-,还原产物为NH3;
b.在碱性条件下,用铝粉还原NO3-,还原产物为N2。
(1)方案a中,生成34g NH3的同时生成__________mol Fe(OH)3。
(2)方案b中发生的反应如下(配平该反应离子方程式):
______Al+______NO3-+______OH-===______AlO2-+______N2↑+______H2O
(3)方案b中,当有0.15 mol电子转移时,生成的氮气在标准状况下的体积为_________mL。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期第一次月考化学试卷(解析版) 题型:实验题
(10分)实验室用密度为1.25 g·mL-1,质量分数为36.5%的浓盐酸配制240 mL 0.1 mol·L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为______________。
(2)配制240 mL 0.1 mol·L-1的盐酸应量取浓盐酸体积________ mL,应选用容量瓶的规格为________mL。
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)________。
A.用30 mL水洗涤 2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用________加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线________处
(4)操作A中,将洗涤液都移入容量瓶,其目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com