
【题目】现有淀粉溶液、鸡蛋清、葡萄糖溶液,区别它们时,下列试剂和对应现象依次是( )
试剂:①新制的Cu(OH)2 ②碘水 ③浓硝酸
现象:a.变蓝色 b.红色沉淀 c.变黄色
A. ②—a、①—c、③—b B. ③—a、②—c、①—b
C. ②—a、③—c、①—b D. ②—c、③—a、①—b
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法中正确的是 ( )
A. 标准状况下,9g H2O所占的体积为11.2L
B. 1 mol OH-所含的电子数为8NA
C. 标准状况下,28 g CO和N2的混合气体的体积为22.4L
D. 0. 5NA个H2所含的体积为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li—CuO二次电池的比能量高、工作温度宽,性能优异,广泛应用于军事和空间领域。
(1)Li—CuO电池中,金属锂做_______极 。
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣。比较Li、Na、Al分别作为电极时比能量的大小:____________。
(3)通过如下过程制备CuO。
![]()
①过程Ⅰ,H2O2的作用是__________________。
②过程Ⅱ产生Cu2(OH)2CO3的离子方程式是_____________________。
③过程Ⅱ,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%。
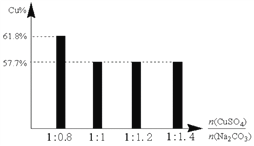
二者比值为1:0.8时,产品中可能含有的杂质是_____________,产生该杂质的原因是_________________________________。
④ 过程Ⅲ反应的化学方程式是_________________________。
(4)Li—CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理示意如下。放电时,正极的电极反应式是______________________。
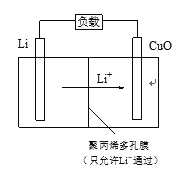
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,错误的是
A. 化学的特征就是认识分子和制造分子,它是一门具有创造性和实用性的科学
B. 人们可以利用化学变化制造出新的原子和新的分子
C. 制陶、冶金及酿酒等过程中发生了化学变化
D. 化学家可以利用化学变化制造出自然界中不存在的物质,制造出“第二自然界”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列判断正确的是
A. 常温下,pH=1的盐酸溶液中,由水电离的H+个数为10-13NA
B. 标准状况下,氧原子总数为0.2NA的CO2和NO2的混合气体,其体积为2.24L
C. 常温下,5.6g铁分别与足量氯气和浓硝酸反应,转移的电子数目均为0.3NA
D. 100g46%(质量分数)乙醇溶液中所含O-H数目为7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 同分异构体的相对分子质量相同,结构不同,化学性质一定相似
B. 可以用新制的Cu(OH)2悬浊液检验尿液中是否含糖
C. 向鸡蛋清溶液中加入(NH4)2SO4饱和溶液,有沉淀析出,再加水沉淀不溶解
D. 油脂、糖类和蛋白质是食物含有的主要营养物质,它们都是高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
I.氮氧化物的研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应: 2NO(g)+O2(g) ![]() 2NO2(g),下列状态能说明该反应达到化学平衡的是_______
2NO2(g),下列状态能说明该反应达到化学平衡的是_______
A.混合气体的密度保持不变 B.NO的转化率保持不变
C.NO和O2的物质的量之比保持不变 D.O2的消耗速率和NO2的消耗速率相等
(2)已知反应:2NO(g) ![]() N2(g)+O2(g) ΔH<0,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
N2(g)+O2(g) ΔH<0,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
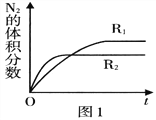
A.压强 B.温度 C.催化剂
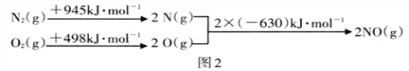
根据如图中的能量变化数据,计算反应:
2NO(g) ![]() N2(g)+O2(g) 的ΔH=__________
N2(g)+O2(g) 的ΔH=__________
II.碳氧化物的研究
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) ΔH<0,现在体积为1L的恒容密闭容器(如图甲)中通入1molCO和2molH2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<0,现在体积为1L的恒容密闭容器(如图甲)中通入1molCO和2molH2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:

请回答:
①T1_____ T2(填“>”或“<”或“=”),理由是____________________。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为_________,该温度下的化学平衡常数为________ 。
②若将1molCO和2molH2通入原体积为1L的恒压密闭容器(如图乙)中,在T2℃下达到平衡,此时反应的平衡常数为_________;若再向容器中通入l mol CH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量_________(填“变大”或“变小”或“不变”)。
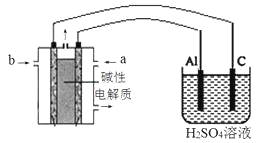
③以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池。以此电池作电源,在实验室中模拟铝制品表面“钝化”处理过程(装置如图所示)。其中物质b是________,阳极电极反应为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茶是我国的传统饮品,茶叶中含有茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )
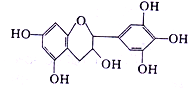
①分子式为C15H14O7 ②1mol儿茶素A在一定条件下最多能与7mol H2加成 ③等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1:1 ④1mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4mol
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com