
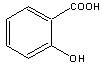
 + (CH3CO)2O
+ (CH3CO)2O 
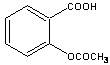 + CH3COOH
+ CH3COOH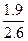 ×100%=73%。
×100%=73%。

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:不详 题型:实验题
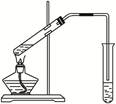
 仪器如图所示(装置可重复使用)。回答下列问题:
仪器如图所示(装置可重复使用)。回答下列问题: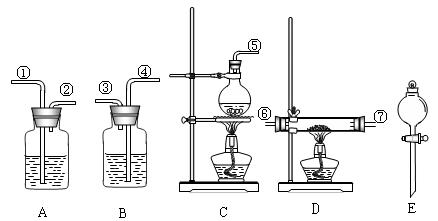
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
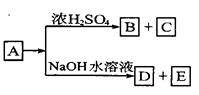
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢氧化钙乳浆 | B.碳酸钠溶液 | C.碳酸氢钠溶液 | D.氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.检验C2H5Cl中的氯元素时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸进行酸化 |
| B.为了提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液进行酸化 |
| C.鉴别待测液是否含有Fe2+时,用HNO3酸化 |
| D.进行乙醛银镜反应时,常在新配制的银氨溶液中,滴入少量稀NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ |
| B.②⑥ |
| C.④⑤ |
| D.③⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com