
����Ŀ��NaClO2��һ����Ҫ��ɱ����������Ҳ������Ư��֯��ȣ���һ������������ͼ���ش��������⣺ 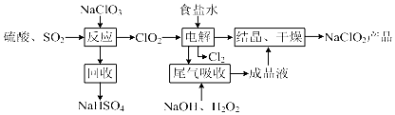
��1��ClO2�ķе�Ϊ283K����ClO2�ֽⱬը��һ����ϡ����������ϡ�͵�10%���¸���ȫ��д������Ӧ������������ClO2�Ļ�ѧ����ʽ ��
��2����β�����ա������ա���⡱�����ų�������ClO2 ��
����β�����չ����У��ɴ���H2O2���Լ���������ţ���
A��Na2O2B��Na2S C��FeCl2D��KMnO4
�����β��������Ч�ʵĿ��д�ʩ��������ţ���
A��β������ʱ��ֽ�������ҺB���ʵ��ӿ�β����ͨ������C�����¶ȿ�����20������D����ˮϡ��β������Һ
�۴����շ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ ��
��3���ڼ�����Һ��NaClO2�Ƚ��ȶ�����������Һ�У�ClO2����H+��ΪHClO2 �� HClO2
��Ψһ����±�ᣬ���ȶ����ֽ����Cl2��ClO2��H2O��д��HClO2�ֽ�Ļ�ѧ����ʽ�� ��
��4����֪NaClO2���ܽ�����¶����߶�����NaClO2������Һ��38������60�����»�����NaClO2 �� ��NaClO2���������п��ܻ��е����������ѧʽ����
���𰸡�
��1��2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2
��2��C��AC��2��1
��3��8HClO2=Cl2��+6ClO2��+4H2O
��4��NaCl��Na2SO4
���������⣺��1��NaClO3��SO2��H2SO4�ữ����������ClO2 �� ����NaClO2������������ԭ����ΪNaCl�����ղ���ΪNaHSO4 �� ˵�������������ƣ��Ҳ���ClO2 �� ���ݵ����غ��֪���˷�Ӧ�Ļ�ѧ����ʽΪ��2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2 ��
���Դ��ǣ�2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2����2������β�����չ����У��������������������Һ����ClO2 �� ����ΪClO2�� �� ��H2O2Ϊ��ԭ�����ֲ��������µ����ʣ����Կɴ���H2O2���Լ���Na2O2 �� ��ѡ��A��
�����β��������Ч�ʣ�����Խ��衢����β����ͨ�����ʡ���������ҺŨ�ȣ���ClO2�ķе�Ϊ283K�����Խ��¶ȿ�����20������Ҳ�������β��������Ч�ʣ���ѡ��AC��
����ͼ��֪�����ú��������������������Һ����ClO2 �� ����ΪClO2�� �� ��˷�Ӧ��ClO2Ϊ����������ԭ����ΪClO2�� �� ���ϼ۴�+4�۽�Ϊ+3�ۣ�H2O2Ϊ��ԭ������������ΪO2 �� ÿĦ��H2O2�õ�2mol���ӣ����ݵ����غ��֪�������ͻ�ԭ�������ʵ���֮��Ϊ2��1��
���Դ��ǣ�2��1����3��HClO2���ȶ����ֽ����Cl2��ClO2��H2O�����ݵ����غ��֪���ֽ�Ļ�ѧ����ʽΪ8HClO2=Cl2��+6ClO2��+4H2O�����Դ��ǣ�8HClO2=Cl2��+6ClO2��+4H2O����4�����Ʊ����̿�֪�����������ΪClO2�Ͷ���SO2���壬�������ú��������������������Һ����β��ClO2�Ͷ���SO2���壬����ΪClO2�� �� ��������Na2SO4 �� �������ᾧ���������Һ���˺�NaClO2������NaCl��Na2SO4 �� ��NaCl��Na2SO4 ���ܽ�����¶����߶���������38������60�����»�����NaClO2ʱ���ܻ��е�������NaCl��Na2SO4 �� ���Դ��ǣ�NaCl��Na2SO4 ��


 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д� â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤������������������ȷ���ǣ� ��
A.24gþ��ԭ������������ΪNA
B.1L 0.1molL��1������Һ��H+��Ϊ0.1NA
C.1mol�����������������Ϊ10NA
D.��״���£�22.4L�Ҵ��ķ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.��ѧ��Ӧ���ʱ��뷴Ӧ��;���й�
B.�����£�ϡ��0.1molL��1CH3COOH��Һ����Һ�ĵ�����������
C.���³�ѹ�£�22.4L Cl2�к��еķ�����Ϊ6.02��1023��
D.��������ͭ��a��b����;����ȫת��ΪCu��NO3��2 �� ;��a��b���ĵ�����һ����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
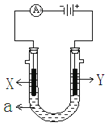
��1����X��Y����ʯī�缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ���ٵ�����X���ϵĵ缫��ӦʽΪ_______________________����X�������۲쵽��������___________________��
��Y�缫�ϵĵ缫��ӦʽΪ__________________________��һ��ʱ���������Һ�п�����ʵ��������_________________________��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ������
��X�缫�IJ�����_______________���缫��Ӧʽ��______________________��
��Y�缫�IJ�����______________���缫��Ӧʽ��__________________��(˵�������ʷ����ĵ缫��Ӧ����д��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦA��g��+3B��g��2C��g��+2D��g����4�ֲ�ͬ����·�Ӧ���ʷֱ����£����з�Ӧ����v�����ǣ� ��
A.v��A��=9.0mol/��Lmin��
B.v��B��=0.6 mol/��Ls��
C.v��C��=0.3 mol/��Ls��
D.v��D��=0.1 mol/��Ls��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ���У�U����Ϊ��īˮ��a��b�Թ��зֱ�ʢ��ʳ��ˮ���Ȼ����Һ����֪�Ȼ����Һ�����ԣ��������������飬����һ��ʱ�䣮�����й�����������ǣ� �� 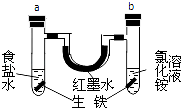
A.a�з�����������ʴ��b�з��������ⸯʴ
B.a��������Ӧ����ʽ�ǣ�O2+2H2O+4e���T4OH��
C.a��b�Թ�������������������صĸ���
D.��īˮ��һ��ʱ�������Һ���Ϊ����Ҹ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������;��˵���У�����ȷ����
A. HNO3�����ƻ��ʡ�ũҩ B. NH3�������
C. Fe3O4������ɫ�����Ϳ�� D. Na2O2����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ�������屽�ķϴ���FeBr3��ԭ�ϣ���ȡ��ı���Һ����ˮFeCl3 �� ��������ܴﵽ��Ӧʵ��Ŀ���ǣ� �� 
A.��װ�ü���ȡ����
B.��װ��������FeBr3��Һ�е�������
C.��װ�ñ���Һʱ�ȴ��¿ڷų�ˮ�࣬�ٴ��Ͽڵ����л���
D.��װ�ö�����Һ���ˮ���������ɣ��������Ƶ���ˮFeCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����п������ж�ij����Ϊ����ķ����ǣ� ��
A.����B.�������C.�˴Ź���D.X�������䷨
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com