
| A. | 4种 | B. | 6种 | C. | 10种 | D. | 14种 |
分析 含有两个或两个以上取代基的同分异构体书写,若只凭想象写很容易造成重、漏现象.不如先将所有取代基拿下,分析母体对称性找出被一个取代基取代的产物种类,然后再分析各种一取代物的对称性,看第二个取代基可进入的位置,…,直至全部取代基都代入.
解答 解:第一步:苯环上有1个取代基时,只有一种结构;
第二步:苯环上有2个取代基时,把一个取代基置于1位,则另一个取代基有2、3、4三种连接方式,即有临、间、对3种同分异构体.且与2个取代基是否相同无关;
第三步:环上有3个取代基,先将2个取代基分别定于临、对、间三种位置,第三个取代基共有4+4+2=10种连接方式,故有10种同分异构体.
故选C.
点评 分子的对称性与苯环上的取代基种类和数目有关,这也决定了多个取代基在苯环上变换位置所形成同分异构体的数目.


科目:高中化学 来源: 题型:选择题
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物可以分解为PH3和HI | |
| C. | 这种化合物不能跟碱反应 | |
| D. | 该化合物中每个原子的最外层都满足8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最简式相同的各物质必定互为同分异构体,互为同分异构体的物质最简式也相同 | |
| B. | 组成元素相同且各元素质量分数也相同的一定互为同分异构体 | |
| C. | 有相同的分子通式且分子组成上相差一个或若干个CH2原子团的物质一定互为同系物 | |
| D. | 分子式相同的不同有机物,一定是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)?5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示.下列说法正确的是( )
利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)?5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示.下列说法正确的是( )| A. | b点时,CO的转化率为20% | |
| B. | 容器内的压强保持恒定,表明反应达到平衡状态 | |
| C. | b点和d点的化学平衡常数:Kb>Kd | |
| D. | 0到0.5min反应速率V(CO)=0.3mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
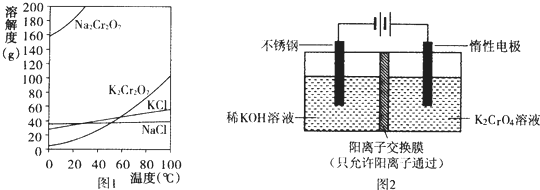
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
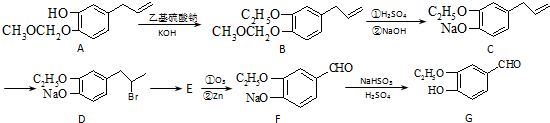
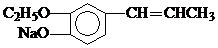 .
.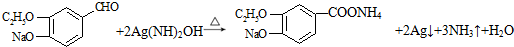 .
.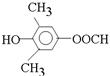 或
或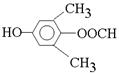 .
.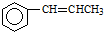 为原料制备
为原料制备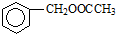 的合成路线流程图(无机试剂任用).合成路线流程图示例如下
的合成路线流程图(无机试剂任用).合成路线流程图示例如下查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B>A>C | B. | A>C>B | C. | A>B>C | D. | B>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
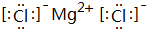 ,其中所含化学键的类型是离子键.
,其中所含化学键的类型是离子键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3 Fe2O3 | B. | Fe(OH)2 Fe2O3 | C. | Fe(OH)2 Fe(OH)3 | D. | Fe(OH)2 Fe3O4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com