
| A. | c(Ba2+)=c(SO42-) | |
| B. | c(Ba2+)增大,c (SO42-) 减小 | |
| C. | c(Ba2+)≠c SO42-),c(Ba2+)•c(SO42-)=KSP(BaSO4) | |
| D. | c(Ba2+)≠c(SO42-),c(Ba2+)•c(SO42-)≠KSP(BaSO4) |
分析 常温下,在BaSO4饱和溶液中存在溶解平衡BaSO4(s)?Ba2+(aq)+SO42-(aq),向硫酸钡饱和溶液中加入Na2SO4固体,Na2SO4电离出SO42-而抑制BaSO4溶解,结合电荷守恒分析解答.
解答 解:常温下,在BaSO4饱和溶液中存在溶解平衡BaSO4(s)?Ba2+(aq)+SO42-(aq),向硫酸钡饱和溶液中加入Na2SO4固体,Na2SO4电离出SO42-而抑制BaSO4溶解,
A.溶液中存在电荷守恒c(Na+)+2c(Ba2+)=2c(SO42-),所以存在c(Ba2+)<c(SO42-),故A错误;
B.Na2SO4电离出SO42-而导致c(SO42-)增大,抑制BaSO4溶解,则c(Ba2+)减小,故B错误;
C.根据A知,c(Ba2+)<c(SO42-),所以c(Ba2+)≠c SO42-),硫酸钡溶度积常数KSP(BaSO4)=c(Ba2+)•c(SO42-),故C正确;
D.根据C知,存在c(Ba2+)≠c SO42-),c(Ba2+)•c(SO42-)=KSP(BaSO4),故D错误;
故选C.
点评 本题考查离子浓度大小比较,为高频考点,明确难溶物溶解平衡影响因素是解本题关键,注意:溶度积常数只与温度有关,与离子浓度大小无关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 等于15% | B. | 大于15% | C. | 小于15% | D. | 无法估算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{2}$lg($\frac{b}{a}$) | B. | $\frac{1}{2}$lg($\frac{a}{b}$) | C. | 14+$\frac{1}{2}$lg($\frac{a}{b}$) | D. | 14+$\frac{1}{2}$lg($\frac{b}{a}$) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3 04 | B. | CuO | C. | HgS | D. | FeS |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
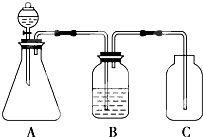
| A. | A中的化学反应可能为:CaCO3+2HCl═CO2↑+CaCl2+H2O | |
| B. | 装置B中盛放的试剂为Na2CO3溶液 | |
| C. | 装置C中盛放的为可溶性硅酸盐 | |
| D. | 由此实验可得到的结构是:酸性HCl>H2CO3>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
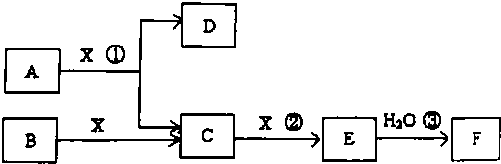
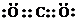 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | R | D |
| 相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期I B族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
| 键能(kJ/mol) | 熔点(K) | 沸点(K) | |
| BO2 | B-O:452 | 1923 | 2503 |
| DO2 | D=O:615,D-O:348 | 216 | 195 |
 ,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$.
,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$. ( AH3配体作为一个整体写).
( AH3配体作为一个整体写).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100g溶液中含有0.9g NaCl | B. | 100g水中含有0.9g NaCl | ||
| C. | 100g溶液中含有0.9mol NaCl | D. | 100g水中含有0.9mol NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com