



科目:高中化学 来源: 题型:
| A、物质的量和摩尔是两个不同的物理量 |
| B、摩尔是物质的量的单位,1摩尔任何物质含6.02x1023个原子 |
| C、阿伏伽德罗常数是人们规定的数,没有单位 |
| D、当H2的摩尔质量以g.mol-1为单位时,在数值上与H2的相对分子质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
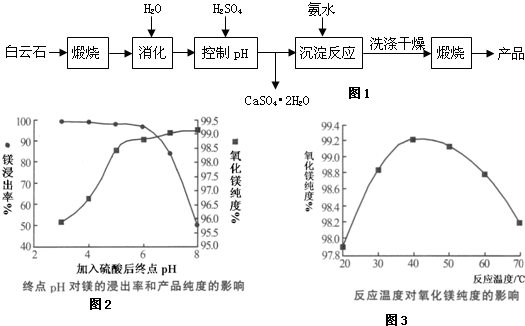
查看答案和解析>>
科目:高中化学 来源: 题型:
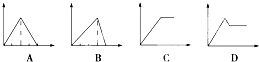
查看答案和解析>>
科目:高中化学 来源: 题型:
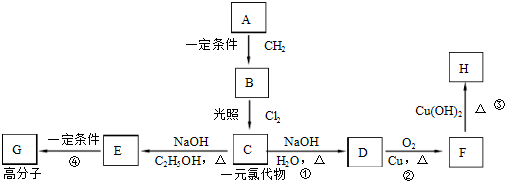
查看答案和解析>>
科目:高中化学 来源: 题型:
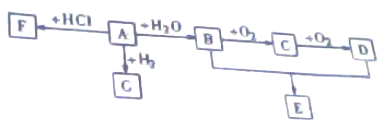
查看答案和解析>>
科目:高中化学 来源: 题型:
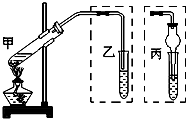 如图在甲处的试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入5mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在乙处的试管中加入5mL饱和碳酸钠溶液,按图连接好装置,用酒精灯对甲处的试管缓慢加热,当观察到乙处的试管中有明显现象时停止实验.请回答:
如图在甲处的试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入5mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在乙处的试管中加入5mL饱和碳酸钠溶液,按图连接好装置,用酒精灯对甲处的试管缓慢加热,当观察到乙处的试管中有明显现象时停止实验.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用丁达尔现象区别蔗糖溶液和淀粉溶液 |
| B、用燃着的木条鉴别CO2和O2 |
| C、用稀硫酸鉴别锌片和铜片 |
| D、用加水溶解的方法即可鉴别食盐和白糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com