
��12�֣�����ͭ���ʼ��仯����Ӧ�÷�Χ�ܹ㡣���к��Ȼ��������ʵ��Ȼ�ͭ����(CuCl2��2H2O)�� Ϊ��ȡ������CuCl2��2H2O�����Ƚ����Ƴ�ˮ��Һ��Ȼ����ͼ��������ᴿ��

��֪Cu2+��Fe3+��Fe2+���������↑ʼ�����ͳ�����ȫʱ��pH�����±���
Fe3+ | Fe2+ | Cu2+ | |
�������↑ʼ����ʱ��pH | 1.9 | 7.0 | 4.7 |
����������ȫ����ʱ��pH | 3.2 | 9.0 | 6.7 |
��ش��������⣺
��1���õ���ҺII�������������X, ���ʺ���������X���� ��
A��K2Cr2O7 B��NaClO C��H2O2 D��KMnO4
��2������������X��Ŀ���� ��
��3��Ϊ�˳�ȥFe3+�����������Y������Һ��PHֵΪ
��4������ܲ���ֱ�������ᾧ�õ�CuCl2��2H2O����? (��ܡ����ܡ�)�����ܣ����ûش������ܣ��ش����β���? ��
��5����֪Fe(OH)3��Ksp=1��10-35mol4/L4 ����Fe3+������ȫʱ������Һ��Fe3+��Ũ��Ϊ1��10-5mol/L�� ���ʱ��Һ��PH��СΪ .
��1��C��2�֣���2����Fe2+������Fe3+����������Fe(OH)3��������Cu2+���룻��2�֣���3��3.2-4.7֮�䣨2�֣���4�����ܣ�2�֣� Ӧ��HCl�����м��������ᾧ��2�֣���5��4��2�֣�
��������
����������������֪������������Ϊ�˳�ȥ�Ȼ�ͭ�����е��Ȼ��������ʣ����ݱ����е����ֽ������ӳ�����pH��֪Fe3+�����׳���������Fe3+������ȫʱCu2+������������Ǽ���������X��Fe2+ת��ΪFe3+�����ܳ�ȥ���ʣ�Ϊ���ܰ�Fe2+����Ϊ Fe3+���������µ����ʣ�������Ӧѡ��H2O2����1������������֪��X��H2O2����2������H2O2��Ŀ���ǽ�Fe2+������Fe3+����������Fe(OH)3��������Cu2+���룻��3��������ҺpHʱҪ����Fe3+��ȫ��������СҪ�õ�3.2����������Cu2+���������ܴﵽ4.7������pH��3.2��4.7֮�䡣��4��CuCl2��ǿ�������Σ����ֱ�������ᾧCuCl2����ȫˮ�⣬���õ�����Cu��OH��2�����Բ���ֱ�������ᾧ��Ҫ�õ�CuCl22H2O�ľ����Ҫ��ȡ��ʩ����CuCl2��ˮ�⣬��ô��������HCl�Ļ����м��������ᾧ����5��Fe(OH)3��Ksp=c(Fe3+)��c3��OH-��=1��10-35mol/L���������ӳ�����ȫʱ��Һ��Fe3+��Ũ��Ϊ1��10-5mol/L������1��10-5��c3��OH-��=1��10-35���ã�c��OH-��=1��10-10mol/L����c(H+)=10-4mol/L����pH=4��
���㣺������Ļ������ⷽ��������ˮ���Ӧ�á��ܶȻ��ļ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�����ѧ����Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
�ۻ�ѧ�Dѡ��5���л���ѧ�����ݣ�15�֣��ܻ�����Ҫ�������ϵ����ܼ���Ҳ����Ϊũҩ���塢������ͻ�ױƷ�ȵ�ԭ�ϡ������ܻ�����DBP���ɸ��ưƵ����ϵĿڸУ��������涨�����������������˺�����ϳ���·ͼ��ͼI��ʾ��
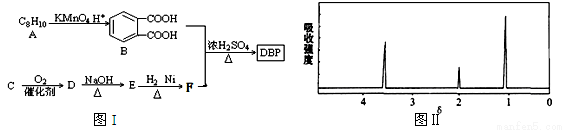
��֪������Ϣ��
��
��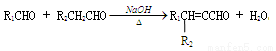 ����R1��R2��ʾ��ԭ�ӻ�������
����R1��R2��ʾ��ԭ�ӻ�������
��CΪ������̼ԭ�ӵ����ĺ����������˴Ź�������ͼ��ͼII��ʾ
��1��C�Ľṹ��ʽΪ ��E�����������ŵ������� ��
��2��д�������йط�Ӧ�Ļ�ѧ����ʽ��
��E��H2�����ʵ�����1�U1��Ӧ����F�� ��
��B��F�����ʵ�����1�U2�ϳ�DBP�� ����Ӧ����Ϊ ��
��3��ͬʱ��������������B��ͬ���칹���� �֣�д��������������ͬ���칹��Ľṹ��ʽ ��
�ٲ��ܺ�NaHCO3��Һ��Ӧ ���ܷ���������Ӧ
����FeC13��Һ����ɫ �ܺ˴Ź���������ʾ������ֻ��һ����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�����ѧ����������ۻ�ѧ�Ծ� �������棩 ���ͣ������
��14�֣��ס��ҡ����dz������������ʣ�����֮������ͼ��ʾ��ת����ϵ������Ҫ��ش����⣺
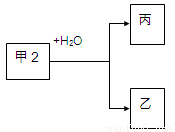
I����֪�����dz������ʣ���Ϊ������
��1������Ϊ���������д��ԣ����ҷ������ȷ�Ӧ�Ļ�ѧ����ʽΪ ��
��2������Ϊ̼��������ҡ����ɺϳɼ״���
����֪��CH4(g)��H2O(g) CO(g)��3H2(g) ��H����206.0 kJ��mol��1
CO(g)��3H2(g) ��H����206.0 kJ��mol��1
CH4(g)��H2O(g) CH3OH(g)��H2(g) ��H����77.0 kJ��mol��1
CH3OH(g)��H2(g) ��H����77.0 kJ��mol��1
д�����������������Ӧ����CH3OH(g)���Ȼ�ѧ����ʽ��__________________��
���Һͱ��ϳɼ״��ķ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)���±�����T1 ______ T2���>������<������=������
�¶�/�� | T1 | T2 |
K | 2.041 | 0.012 |
���ҿ���ij����ȼ�ϵ�ص�ȼ�ϣ��õ�صĸ�����ӦʽΪ_________________��
II����֪�����������ֶ�����Ԫ����ɵĻ��������ˮ��Һ�Լ��ԡ�
��3�������ɼ����������Ӹ�����Ϊ2:3���������塣�ɼ����������Ӱ뾶��С��ϵΪ ���þ��������ʾ����
��4��������O2�����һ����Ҫ��;�� ���������Cl2��2:1�����ʵ�������Ӧ�õ�����Һ������Һ��������Ũ�ȴӴ�С��˳���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��������ɽ����ѧ�ڸ�һ��ѧ��ĩ�Ծ��������棩 ���ͣ�ѡ����
ij��Һ�м���������������ų������ڴ���Һ�п��ܴ��������������
A��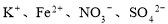 B��
B��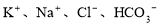
C��K+��Na+��AlO2-��SO42- D��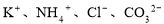
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��������ɽ����ѧ�ڸ�һ��ѧ��ĩ�Ծ��������棩 ���ͣ�ѡ����
�����й���ɫ��Ӧ��˵���������
A���۲�K2SO4����ɫӦ����ɫ���ܲ���
B��Na��NaCl������ʱ������ɫ��ͬ
C����������ɫ��Ӧ������NaCl��KCl
D����ɫ��Ӧһ��������ѧ�仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��ͷ�е���У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ���й����ʵ�Ũ�ȹ�ϵ��ȷ����
A��c(NH4��)��ȵ�(NH4)2SO4��NH4HSO4��NH4Cl��Һ�У�c(NH4HSO4) > c[(NH4)2SO4]> c(NH4Cl��
B�����������Һ�м����������ᣬ�õ������Ի����Һ��c(Na��)��c(CH3COO��)��c(H��)��c(OH��)
C��1.0 mol/L Na2CO3��Һ��c(OH��)��c(HCO3��)��c(H��)��2c(H2CO3)
D��ij��Ԫ������ʽ��NaHA��Һ�У�c(H+����c(Na������c(OH������c(HA������2c(A2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��ͷ�е���У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���£�ij��Һ����ˮ���������c(H+)=10��12�������и��������ڸ���Һ��һ�����Դ����������
A��K+��Na+��AlO2����Cl�� B��Na+��Cl����SO42����HCO3��
C��NH4+��Na+��NO3����SO42�� D��Ba2+��Na+��Cl����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼ��ʵ��װ���У�ʵ�鿪ʼһ��ʱ��Կ�����������������ȷ����
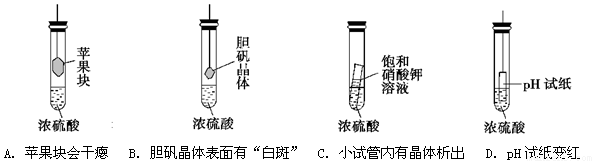
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ�����и߶���ѧ����ĩ���Ի�ѧ���Ծ��������棩 ���ͣ�?????
��NA��ʾ�����ӵ�������ֵ������������ȷ����
A��1molH2O�к��е�ԭ����ΪNA
B��2gH2�к��е���ԭ����Ϊ2NA
C�����³�ѹ�£�11.2LN2�к��еķ�����Ϊ0.5NA
D��1L0.1mol��L-1 NaNO3��Һ�к��е���������ΪNA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com