
 £»
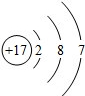
£»·ÖĪö £Ø1£©øł¾ŻŗĖĶāµē×ÓÅŲ¼¹ęĀÉŠ“³öClŌ×Ó½į¹¹Ź¾ŅāĶ¼£»
£Ø2£©øł¾Ż2FeCl3+Cu=CuCl2+2FeC12£¬½«CuøÆŹ“Ņ»°ėŹ±£¬ĖłŅŌČÜŅŗÖŠ³żĮĖÉś³ÉĪļŅŌĶā»¹ÓŠ·“Ó¦ĪļŹ£Óą£¬¾Ż“Ė·ÖĪö£»
£Ø3£©øł¾Ż2FeCl3+Cu=CuCl2+2FeC12£¬½įŗĻ½«Ä³µēĀ·°åÉĻµÄCuøÆŹ“ĶźČ«£¬Ē”ŗĆĻūŗÄ0.5L2mol/LFeCl3¼ĘĖć£»
£Ø4£©øł¾ŻŌŁÉśFeC13£ŗ2FeC12+C12=2FeC13£¬¼“¶ž¼ŪĢś×Ŗ±ä³ÉČż¼ŪĢśÅŠ¶ĻČÜŅŗŃÕÉ«±ä»Æ£¬øł¾ŻČÜŅŗÖŠ¶ž¼ŪĢśµÄ×ÜĮæ¼ĘĖćĻūŗĵÄCl2£®
½ā“š ½ā£ŗ£Ø1£©ClµÄÖŹ×ÓŹżĪŖ17£¬Ō×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ£ŗ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø2£©ŅņĪŖøÆŹ“Cu£ŗ2FeCl3+Cu=CuCl2+2FeC12£¬½«CuøÆŹ“Ņ»°ėŹ±£¬ĖłŅŌČÜŅŗÖŠ³żĮĖÉś³ÉFe2+”¢Cu2+ŅŌĶā»¹ÓŠFe3+Ź£Óą£¬¶ųc£ØCl-£©²»±ä¼“2mol/L”Į3=6mol/L£¬
¹Ź“š°øĪŖ£ŗFe2+”¢Fe3+”¢Cu2+£»6£»
£Ø3£©ŅņĪŖøÆŹ“Cu£ŗ2FeCl3+Cu=CuCl2+2FeC12£¬½«Ä³µēĀ·°åÉĻµÄCuøÆŹ“ĶźČ«£¬Ē”ŗĆĻūŗÄ0.5L2mol/LFeCl3£¬ĖłŅŌøÆŹ“µÄCuµÄ×ÜĪļÖŹµÄĮæĪŖ0.5L”Į2mol/L”Į$\frac{1}{2}$=0.5mol£¬¹Ź“š°øĪŖ£ŗ0.5£»
£Ø4£©ŌŁÉśFeC13£ŗ2FeC12+C12=2FeC13£¬¼“¶ž¼ŪĢś×Ŗ±ä³ÉČż¼ŪĢś£¬ĖłŅŌČÜŅŗÓÉĒ³ĀĢÉ«×īÖÕ±äĪŖ»ĘÉ«£¬øł¾ŻøÆŹ“Cu£ŗ2FeCl3+Cu=CuCl2+2FeC12£»
Č»ŗó»ŲŹÕCu£ŗFe+CuCl2=Cu+FeCl2£»Ōņ×īÖÕ¶ž¼ŪĢśĄė×ÓµÄĪļÖŹµÄĮæĪŖ0.5L”Į2mol/L+0.5L”Į2mol/L”Į$\frac{1}{2}$=1.5mol£¬ŌņĻūŗĵÄCl2ŌŚ±ź×¼×“æöĻĀµÄĢå»żÖĮÉŁĪŖ1.5mol”Į22.4L/mol=16.8L£»
¹Ź“š°øĪŖ£ŗĒ³ĀĢ£»»Ę£»16.8£®
µćĘĄ ±¾Ģāæ¼²éÓ”Ė¢µēĀ·°å²¢ŌŁÉśµÄĻą¹ŲĪŹĢā£¬ÄŃ¶Č²»“ó£¬Ć÷Č·ĪļÖŹŠŌÖŹ”¢ĪļÖŹ·“Ó¦¹ż³ĢŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢ŅāŌŖĖŲ»ÆŗĻĪļÖŖŹ¶µÄ»żĄŪ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ś¢Ü¢Ü¢Ž | D£® | Č«²æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌČÜŅŗÖŠæÉÄÜŗ¬ÓŠK+£¬Ņ»¶ØƻӊHCO3-ŗĶOH-£¬½«²śÉśµÄĪŽÉ«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®ÖŠ£¬³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē | |
| B£® | ŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠCl-ŗĶNO3-£¬æÉÄÜŗ¬ÓŠSO42-£¬·“Ӧɜ³ÉµÄĪŽÉ«ĘųĢåÓöæÕĘų±äŗģ×ŲÉ« | |
| C£® | ŌČÜŅŗÖŠĖłŗ¬µÄŃōĄė×ÓĪŖMg2+”¢Fe2+£¬¼ÓČėĻ”ŃĪĖįĖł·¢ÉśµÄ·“Ó¦ĪŖ3Fe2++4H++NO3-ØT3Fe3++NO”ü+2H2O | |
| D£® | ČōĻņŌČÜŅŗÖŠ¼ÓČė¹żĮæNaOHČÜŅŗ£¬½«ĖłµĆ³Įµķ¹żĀĖ”¢Ļ“µÓ”¢×ĘÉÕµ½ŗćÖŲ£¬µĆµ½µÄ¹ĢĢåÖŹĮæĪŖ107 g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ČēĶ¼ĪŖŹµŃéŹŅijÅØŃĪĖįŹŌ¼ĮĘæÉĻµÄ±źĒ©µÄÓŠ¹ŲÄŚČŻ£¬ŹŌøł¾Ż±źĒ©ÉĻµÄÓŠ¹ŲŹż¾Ż»Ų“šĻĀĮŠĪŹĢā£ŗ
ČēĶ¼ĪŖŹµŃéŹŅijÅØŃĪĖįŹŌ¼ĮĘæÉĻµÄ±źĒ©µÄÓŠ¹ŲÄŚČŻ£¬ŹŌøł¾Ż±źĒ©ÉĻµÄÓŠ¹ŲŹż¾Ż»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČŻĘ÷ | ČŻ»ż/L | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖłŠčŹ±¼ä/min | |
| C£Øs£© | H2O£Øg£© | H2£Øg£© | ||||
| ¼× | 2 | T1 | 2 | 4 | 3.2 | 2.8 |
| ŅŅ | 1 | T2 | 1 | 2 | 1.2 | 3.0 |
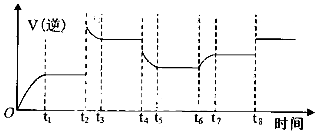
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉĻŹöĮ½ÖÖČÜŅŗ·Ö±šÓĆĖ®Ļ”ŹĶm”¢n±¶£¬ČÜŅŗµÄpH¶¼±ä³É3£¬Ōņm£¾n | |
| B£® | ÉĻŹöĮ½ÖÖČÜŅŗ·Ö±šÓė×ćĮæµÄZnĶźČ«·“Ó¦£¬²śÉśµÄH2Ņ»Ńł¶ą | |
| C£® | ÉĻŹöĮ½ÖÖČÜŅŗ·Ö±šÓėµČÅØ¶ČµÄĒāŃõ»ÆÄĘČÜŅŗĒ”ŗĆ·“Ó¦£¬ĻūŗÄĒāŃõ»ÆÄĘČÜŅŗµÄĢå»żĻąĶ¬ | |
| D£® | 1mol/LµÄŃĪĖįŗĶ1mol/LµÄ“×ĖįµÄ»ģŗĻČÜŅŗÓėĒāŃõ»ÆÄĘČÜŅŗĒ”ŗĆĶźČ«·“Ó¦Ź±£¬·“Ó¦ŗóČÜŅŗÖŠc£ØCH3COO-£©+C£ØCl-£©£¼c£ØNa+£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com