
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、可以用氢氧化铜悬浊液检验甘油和酒精 |
| C、通过化学变化可以实现16O与18O间的相互转化 |
| D、由金属元素和非金属元素形成的化学键一定是离子键 |


科目:高中化学 来源: 题型:
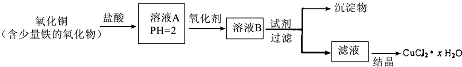
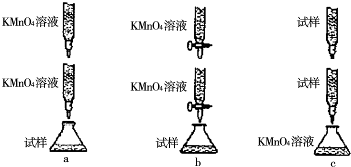
查看答案和解析>>
科目:高中化学 来源: 题型:
127 53 |
131 53 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO(g)+O2(g)=2CO2(g)△H=-566.0 kJ/mol | ||
B、C(s)+
| ||
| C、CH4(g)+2O2(g)=O2(g)+2H2O(l)△H=-890.31 kJ/mol | ||
| D、2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l)△H=-11036 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
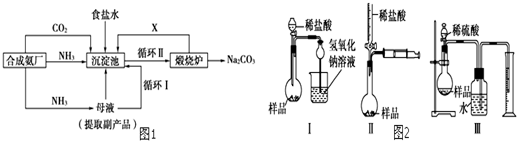
查看答案和解析>>
科目:高中化学 来源: 题型:
 利用如图装置收集以下几种气体(如图中烧瓶位置不得移动)
利用如图装置收集以下几种气体(如图中烧瓶位置不得移动)查看答案和解析>>
科目:高中化学 来源: 题型:
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
| ① |
| ② |
| ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
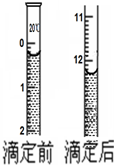 钙是人体神经、骨骼系统等功能功能正常动作所必需的常量元素.某药业公司的钙片包装上有如下说明:
钙是人体神经、骨骼系统等功能功能正常动作所必需的常量元素.某药业公司的钙片包装上有如下说明:| 性状 | 本品为白色片 |
| 贮藏 | 密封,干燥处保存 |
| 规格 | 每片含碳酸钙0.5g(相当于钙0.2g) |
| 包装 | |
| 生产批号 | |
| 生产日期 | |
| 有效期至 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com