
����Ŀ���Ķ����п��ղ��ϲ���ա�
ȼ�ϵ����һ�ֻ�ѧ��أ���������ת���ʸߡ��Ի����Ѻõ��ŵ㡣���磬����ȼ�ϵ���ڹ���ʱ���Ӹ�������ͨ����H2������������ͨ����O2�������ڵ���ڲ�(������H2SO4������KOH�����ʵ���Һ)������Ӧ������H2O��ͬʱ�������ܡ���CH4����C2H5OH��Ҳ������Ϊȼ�ϵ�ص�ȼ�ϡ�Ŀǰ�����Ƴɹ���Al-������ȼ�ϵ�أ������Դ�������Ϊ�����ṩ����Ҳ��������������Դ�ȡ�
(1)���������漰���������У��������������________(����ţ���ͬ)�����ڻ������________��
(2)�����ʵ����������H2��O2��A1������________����������������������Ԫ�ص�һ������������NaOH��Һ��Ӧ�����ӷ���ʽΪ________��
(3)��֪����ȼ�ϵ���з�����ӦΪCH4+2O2=CO2+2H2O����״����ÿ����11.2L���飬ת�Ƶĵ�����ĿΪ________NA��
(4)����ȼ�ϵ�ط����ķ�Ӧ��Ϊ________��Ӧ(�������ԭ����������ԭ��)��
���𰸡��� �� ���� A1(OH) 3+OH-=A1O2-+H2O 4 ������ԭ
��������
(1)������Ԫ����ɣ�����һ������Ԫ�صĻ�������������������������H2O��ѡ�ݣ����ж������ʵ������ǻ��������к��е�����������������̼�ȶ������ʣ��������ڻ���ѡ�
(2)�����ʵ����������H2��O2��A1������һ��Ԫ����ɵĴ���������ڵ��ʣ���������������������Ԫ�ص�һ������������Al(OH)3��Al(OH)3��NaOH��Һ��Ӧ����ƫ�����ƺ�ˮ����Ӧ�����ӷ���ʽΪA1(OH) 3+OH-=A1O2-+H2O��
(3)����ȼ�ϵ���з�����ӦΪCH4+2O2=CO2+2H2O��CH4��CԪ�ػ��ϼ���-4����Ϊ+4����״����ÿ����11.2L���飬ת�Ƶĵ�����ĿΪ![]() 4NA��
4NA��
(4)ԭ���һ���е���ת�ƣ���������ȼ�ϵ�ط����ķ�Ӧ��Ϊ������ԭ��Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���ij�����ܱ������н��з�ӦX(g) + 3Y(g)![]() 2Z(g)����X��Y��Z��ʼŨ�ȷֱ�Ϊc1 mol/L��c2 mol/L��c3 mol/L��c1��c2��c3������0��������Ӧ��ƽ��ʱX��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������жϲ���������
2Z(g)����X��Y��Z��ʼŨ�ȷֱ�Ϊc1 mol/L��c2 mol/L��c3 mol/L��c1��c2��c3������0��������Ӧ��ƽ��ʱX��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������жϲ���������
A. c1��c2 = 1��3
B. ��4v(X)��= v(Y)��ʱ���÷�Ӧ����������Ӧ������ƽ��
C. c1����Ϊ0.1
D. X��Y��ת�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ�ѧ�ұ�����һ��ֱ�ӵ绯ѧ�ϳ�H2O2�ķ�����װ����ͼ��������������ȷ���ǣ� ��
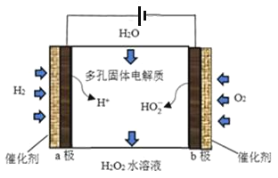
A.��װ�õĹ���ԭ���ǽ���ѧ��ת���ɵ���
B.b�������ĵ缫��ӦΪO2+H2O+2e-=HO2-+OH-
C.��ع���ʱ���ڲ�������Ӧ��HO2-+OH-+2H+=H2O2+H2O
D.��·��ͨ��2mol���ӣ���������22.4L����״����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ��H2Oֻ����ԭ������
A.2H2O![]() 2H2��+O2��B.2F2+2H2O=4HF+O2
2H2��+O2��B.2F2+2H2O=4HF+O2
C.CaO+ H2O=Ca(OH)2D.2Na2O2+2H2O=4NaOH+O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ����������JohnB.Goodenough����λ��ѧ�ң��Ա�������﮵������Ĺ��ס���������ﮣ�LiFePO4����������ӵ���������ϣ��Ʊ�������ͼ��

��1���Ʊ�ˮ����������FePO4��xH2O������
�ٹ��̢�NaOH��Һ��pH=2.0ʱ�������Һ�к�������Ҫ��H2PO4-�����̢�������Ҫ���ӷ���ʽ��____��
�ڹ��̢�����������������Ӧ����FePO4���������ӷ���ʽ��____��
�۽��й���III֮ǰ����ȷ�Ϲ���II����Fe2+�������Լ�Ϊ____��
��FePO4��xH2O��Ʒ������ˮ���̵��������ߣ���Ʒ�������¶ȱ仯�����ߣ���ͼ��

ˮ���������Ļ�ѧʽΪ____����xȡ������
��2���Ʊ�LiFePO4���壺
�ڵ������ձ����£����±���FePO4��Li2CO3���������ǵĹ������
�ٹ���������������____��
������ӵ���ڳ��ʱ���缫����LiFePO4��Ǩ������Li+������ת��ΪLi(1-x)FePO4���˵缫�ĵ缫��ӦΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���п��淴ӦFe(s)+CO2(g) ![]() FeO(s) + CO(g)����֪���¶�938Kʱ��ƽ�ⳣ��K=1.5����1173Kʱ��K=2.2 ��
FeO(s) + CO(g)����֪���¶�938Kʱ��ƽ�ⳣ��K=1.5����1173Kʱ��K=2.2 ��
��1�����жϸ÷�Ӧ�ﵽƽ��״̬��������__________��˫ѡ������ţ���
A��������ѹǿ������ B��c��CO��������
C��v����CO2��=v����CO�� D��c��CO2��=c��CO��
��2���÷�Ӧ������Ӧ��_________��ѡ������������������������Ӧ��
��3��д���÷�Ӧ��ƽ�ⳣ������ʽ__________������ʼʱ��Fe��CO2��������̶����ܱ������У�CO2����ʼŨ��Ϊ2.0mol/L��ij�¶�ʱ�ﵽƽ�⣬��ʱ������CO��Ũ��Ϊ1.0 mol/L������¶���������Ӧ��ƽ�ⳣ��K=__________��������λ��Ч���֣���
��4�����÷�Ӧ������̶����ܱ������н��У���һ�������´ﵽƽ��״̬������ı�������������Ӧ���������CO2�����ʵ���������α仯��ѡ����������������С����������������
�������¶�__________������ͨ��CO___________��
��5���÷�Ӧ���淴Ӧ������ʱ��仯�Ĺ�ϵ����ͼ��

�ٴ�ͼ�п�������Ӧ��t2ʱ��ƽ�⣬ ��t1ʱ�ı���ij���������ı�����������ǣ�����ţ�___________������ѡ��
A������ B������CO2Ũ��
�������t3ʱ�ӻ�����з��������CO��t4~ t5ʱ��η�Ӧ������ƽ��״̬������ͼ�ϻ���t3~ t5��V���棩�仯����______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������±���Ϣ(���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ�)��֪������������ȷ����
Ԫ�ش��� | A | B | C | D | E |
ԭ�Ӱ뾶/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
��Ҫ���ϼ� | +1 | +3 | +2 | +6��-2 | -2 |
A.���Ӱ뾶��С��![]()
B.![]() ��
��![]() �����������������
�����������������
C.����������Ӧˮ����ļ��ԣ�A<C
D.�⻯����ȶ��ԣ�D>E
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ǵ��������ı����������������и�ǿ�������ԣ�ʵ���ҿɽ�����ͨ����ѹ�ŵ������ȡ������3O2![]() 2O3
2O3
��1������������Ӧ����30%������ת��Ϊ���������û������ƽ��Ħ������Ϊ_________ ������һλС������
��2����8L����ͨ���ŵ�ָܺ���ԭ״�����õ�����6.5L�����г���Ϊ__________L��
��3��ʵ���ҽ������ͳ����Ļ������0.896L����״����ͨ��ʢ��20.0gͭ�۵ķ�Ӧ���У���ּ��Ⱥ�ĩ��������Ϊ21.6g����ԭ������г������������Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���ṹ��ʽΪ ��������������ȷ����( )
��������������ȷ����( )
A. 1mol���л����ڼ��Ⱥʹ��������£�����ܺ�4 molH2��Ӧ
B. ���л�����ʹ��ˮ��ɫҲ��ʹ����KMnO4��Һ��ɫ
C. �÷����������9��̼ԭ�ӹ�ƽ��
D. ���л�����һ�������£��ܷ�����ȥ��Ӧ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com