
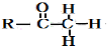 +
+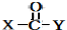 $\stackrel{O{H}^{-}}{→}$
$\stackrel{O{H}^{-}}{→}$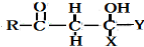
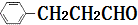 )的路线流程图.路线流程图示例如下:
)的路线流程图.路线流程图示例如下: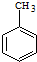 $→_{光}^{Cl_{2}}$
$→_{光}^{Cl_{2}}$ 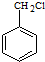 $→_{△}^{NaOH/H_{2}O}$
$→_{△}^{NaOH/H_{2}O}$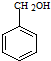
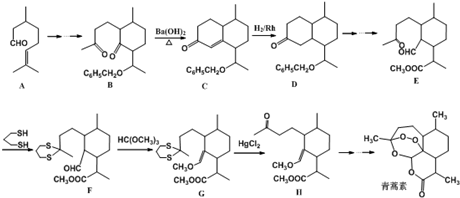
分析 A发生一系列反应生成B,B发生消去反应生成C,C发生加成反应生成D,D发生一系列反应生成E,E发生取代反应生成F,F发生反应生成G,G发生取代反应生成H,H反应一系列反应生成青蒿素,
(1)A.青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有过氧键;
B.青蒿素难溶于水,易溶于乙醇、苯等;
C.青蒿素含有环但不含苯环;
D.酯基能发生水解反应;
(2)化合物A中含有的非含氧官能团的名称是碳碳双键;用新制氢氧化铜悬浊液检验醛基、用稀盐酸将溶液酸化,然后用溴水检验碳碳双键;
(3)由E→F的结构可知,羰基中C=O双键变成C-S单键,由G→H的结构可知C-S单键又变成羰基,目的是保护羰基;
(4)由题目信息可知,结合B、C的结构可知,C=O双键变成C=C双键,应是B中连接羰基的甲基上的α-H与C=O先发生发生加成反应,再发生消去反应生成C;
(5)M与A互为同系物,但比A少两个碳原子,M含有8个C原子且含有碳碳双键和醛基,M的同分异构体符合下列条件:①含有六元环,②能发生银镜反应,说明含有醛基,则六元环上含有1个甲基和1个醛基或1个亚甲基和1个醛基;
(6)CH3CH2Cl在NaOH水溶液中加热发生取代反应生成CH3CH2OH,CH3CH2OH发生催化氧化生成CH3CHO,CH3CHO和苯甲醛反应生成苯丙烯醛,苯丙烯醛发生不完全加成反应生成苯丙醛.
解答 解:A发生一系列反应生成B,B发生消去反应生成C,C发生加成反应生成D,D发生一系列反应生成E,E发生取代反应生成F,F发生反应生成G,G发生取代反应生成H,H反应一系列反应生成青蒿素,
(1)A.青蒿素中含有过氧键,具有强氧化性,能氧化碘离子生成碘,碘遇淀粉变蓝色,所以青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有过氧键,故错误;
B.青蒿素中含有憎水基不含亲水基,所以难溶于水,易溶于乙醇、苯等,故B错误;
C.青蒿素含有环但不含苯环,所以青蒿素属于环状化合物,但不属于芳香族化合物
,故正确;
D.酯基能发生水解反应,故正确;
故选CD;
(2)化合物A中含有的非含氧官能团的名称是碳碳双键;用新制氢氧化铜悬浊液检验醛基、用稀盐酸将溶液酸化,然后用溴水检验碳碳双键,故答案为:碳碳双键;CAB;
(3)由E→F的结构可知,羰基中C=O双键变成C-S单键,由G→H的结构可知C-S单键又变成羰基,目的是保护羰基,
故答案为:保护羰基;
(4)由题目信息可知,结合B、C的结构可知,C=O双键变成C=C双键,应是B中连接羰基的甲基上的α-H与C=O先发生发生加成反应产生C-OH,再发生消去反应生成产生C=C双键生成C,
故答案为:加成反应;消去反应;
(5)M与A互为同系物,但比A少两个碳原子,M含有8个C原子且含有碳碳双键和醛基,M的同分异构体符合下列条件:①含有六元环,②能发生银镜反应,说明含有醛基,则六元环上含有1个-CH3和1个-CHO或1个-CH2-和1个醛基,如果取代基为-CH3和-CHO,有邻间对结构,亚甲基和醛基在同一个碳原子上,只含一个-CH2CHO取代基,所以符合条件的有5种,
故答案为:5;
(6)CH3CH2Cl在NaOH水溶液中加热发生取代反应生成CH3CH2OH,CH3CH2OH发生催化氧化生成CH3CHO,CH3CHO和苯甲醛反应生成苯丙烯醛,苯丙烯醛发生不完全加成反应生成苯丙醛,
其流程图为 ,
,
故答案为: .
.
点评 本题考查有机合成,为高频考点,侧重考查学生分析判断及知识综合应用能力,熟悉常见有机物官能团及其性质、有机反应类型及反应条件是解本题关键,注意醛之间反应断键和成键方式,题目难度不大.


科目:高中化学 来源: 题型:选择题
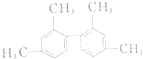
| A. | 等质量的该烃和甲烷均完全燃烧,耗氧量后者小于前者 | |
| B. | 该烃能使酸性高锰酸钾溶液褪色,属于苯的同系物 | |
| C. | 分子中一定有11个碳原子处于同一平面上 | |
| D. | 该烃的一氯取代产物为6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
| 使用填埋法处理未经分类的生活垃圾 | 食用油脂能促进人体对某些维生素的吸收 | 利用二氧化碳可制造全降解塑料,有利于缓解温室效应 | 药皂中的少量苯酚,可起到杀菌消毒的作用 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
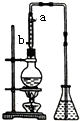 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\underset{\stackrel{{H}^{+}}{→}}{\;}$n(C2H4O).
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\underset{\stackrel{{H}^{+}}{→}}{\;}$n(C2H4O).查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  制取并收集少量HCl | B. | 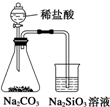 证明非金属性强弱:Cl>C>Si | ||
| C. | 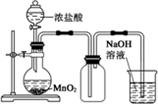 实验室制Cl2 | D. | 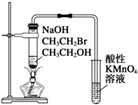 验证溴乙烷发生消去反应生成烯烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com