
| A、一定符合 |
| B、一定不符合 |
| C、两种情况都有可能 |
| D、缺条件无法判断 |
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
| A、向氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
| B、将Al条投入NaOH溶液中:Al+OH-+H2O═AlO2-+H2↑ |
| C、向NaHSO4溶液中滴加Ba(OH)2溶液至恰好为中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| D、澄清石灰水与盐酸反应:Ca(OH)2+2H+═2H2O+Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸与乙醇在浓硫酸作用下加热反应 |
| B、苯和浓硝酸、浓硫酸在50-60℃水浴中加热反应 |
| C、硬脂酸甘油酯在碱性条件下水解得到甘油和肥皂 |
| D、乙烯通入溴的四氯化碳溶液中,溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NF3的形成过程用电子式可表示为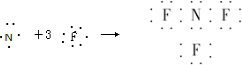 |
| B、NF3的氧化性大于F2 |
| C、NF3分子空间构型为三角锥形 |
| D、NH4F中既有离子键又有极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能使甲基橙变黄的溶液中:Na+、K+、SO42-、AlO2- |
| B、水电离产生的c(H+)=1×10-12mol/L溶液:CH3COOH、Na+、Cl-、I- |
| C、能使pH试纸变深蓝色的溶液中:Na+、AlO2-、S2-、CO32- |
| D、0.1 mol?L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
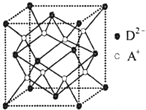 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.谙冋答下列问题:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.谙冋答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
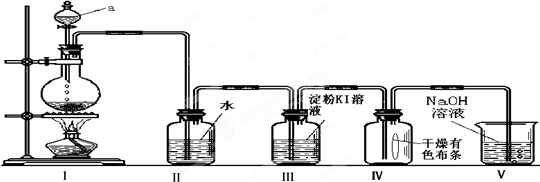
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com