
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“>”“<”或“=”);
(2)830℃时,向一个5L密闭容器中充入0.20 mol A和0.80 mol B,如反应初始6s内A的平均反应速率v(A)=0.003mol·L-1·s-1,则6s时c(A)= mol·L-1,C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为
,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母);
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等

(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为
A(g)+B(g)的平衡常数的值为
(3)a.该反应前后气体的物质的量不变,压强始终不变,故压强不随时间改变,不能说明到达平衡,故a错误, b.混合气体的总质量不变,容器的容积不变,故混合气体的密度始终不变,故气体的密度不随时间改变,不能说明到达平衡,故b错误,c.可逆反应到达平衡时,各组分的浓度不发生变化,故c(A)不随时间改变,说明到达平衡,故c正确,d.单位时间里生成C和D的物质的量相等,都表示正反应速率,反应始终按1:1生成C、D的物质的量,不能说明到达平衡,故d错误,故答案为:c;
(4)同一反应在相同温度下,正、逆反应方向的平衡常数互为倒数,故1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的值为1/0.4=2.5,
考点:化学平衡计算、平衡常数计算、化学反应速率、平衡状态判断


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
已知反应:2CH3COCH3(l)  CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如右图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如右图所示。下列说法正确的是
 A.b代表0℃下CH3COCH3的Y-t 曲线
A.b代表0℃下CH3COCH3的Y-t 曲线
B.反应进行到20min末,CH3COCH3的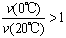
C.升温可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的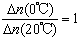
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.68g铁粉加入到30.0mL的1.00 mol·L-1MO2+溶液中,恰好完全反应,向溶液中滴加KSCN溶液,溶液颜色没有变化,则还原产物可能是
A.M B.M+ C.M2+ D.M3+
查看答案和解析>>
科目:高中化学 来源: 题型:
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应说法正确的,下列是
A.弱酸溶液产生较多的氢气
B.强酸溶液产生较多的氢气
C.两者产生等量的氢气
D.无法比较两者产生氢气的量
查看答案和解析>>
科目:高中化学 来源: 题型:
铁镍蓄电池又称爱迪生电池,放电时的总反应为:
Fe+Ni2O3+3H2O==Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe+2OH--2e-==Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-==Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错误的是

装置① 装置② 装置③
A.装置①研究的是电解CuCl2溶液,b电极上有红色固体析出
B.装置②研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e- = Fe2+
C.装置③研究的是电解饱和食盐水, B电极发生的反应:2Cl--2e- = Cl2↑
D.三个装置中涉及的主要反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
为证明Fe3+具有较强的氧化性,甲同学做了如下实验:将Cu片放入0.5mol/L Fe(NO3)3溶液中,观察到Cu片逐渐溶解,溶液由黄色变为蓝绿色,由此甲同学得到Fe3+具有较强氧化性的结论。
乙同学提出了不同的看法:“Fe(NO3)3溶液具有酸性,在此酸性条件下NO3-也能氧化Cu”,并设计实验进行探究。已知:
| 水解反应 | 平衡常数(K) |
| Fe3+ + 3H2O | 7.9 × 10-4 |
| Fe2+ + 2H2O | 3.2 × 10-10 |
| Cu2+ + 2H2O | 3.2 × 10-7 |
请回答:(1)稀硝酸和Cu反应的化学方程式为
(2)请利用所提供的试剂,帮助乙同学完成实验方案设计。
试剂:0.5mol/L Fe(NO3)3溶液、Cu片、精密pH试纸(0.5~5.0)、硝酸钠溶液、稀盐酸。方案:
(3)丙同学分别实施了甲、乙两位同学的实验方案,并在实验过程中用pH计监测溶液pH的变化,实验记录如下。
| 实验内容 | 实验现象 |
| 甲同学的实验方案 | 溶液逐渐变成蓝绿色, pH略有上升 |
| 乙同学的实验方案 | 无明显现象,pH没有明显变化。 |
①据实验现象写出发生反应的离子方程式:
②导致实验过程中溶液pH略有上升的可能原因是
③解释乙同学的实验现象
(4)请你设计更简便可行的实验方案,帮助甲同学达到实验目的:
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)0.5 mol H2O的质量为 ,其中含有 个水分子,共有 个原子。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是 _ ,在相同温度和相同压强条件下,体积最大的是 ,体积最小的是 。
(3)在 mL 0.2 mol/L NaOH溶液中含1 g溶质;配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O ____ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各式中,属于电离方程式的是
A.HCO3-+ H2O  H2CO3 + OH- B.HCO3- + OH- =H2O + CO32-
H2CO3 + OH- B.HCO3- + OH- =H2O + CO32-
C.NH3 + H+=NH4+ D.N
H3·H2O NH4+ + OH-
NH4+ + OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com