
 һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��
һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��| ���� | �¶�/�� | ��ʼ���ʵ���/mol | |
| NO��g�� | CO��g�� | ||
| �� | T1 | 0.20 | 0.20 |
| �� | T1 | 0.30 | 0.30 |
| �� | T2 | 0.20 | 0.20 |
| A�� | �÷�Ӧ������ӦΪ���ȷ�Ӧ | |
| B�� | �ﵽƽ��ʱ������CO2����������ȼ��е�С | |
| C�� | T1��ʱ������ʼʱ����г���0.40molNO��0.40molCO��0.40molN2��0.40molCO2����Ӧ�ﵽ��ƽ��ǰv��������v���棩 | |
| D�� | T2��ʱ������ʼʱ����г���0.06molN2��0.12molCO2�����ƽ��ʱN2��ת���ʴ���40% |
���� A���ȹ���ƽ�¶ȸߣ���ƽ��״̬������̼���ʵ���С��˵���¶�Խ��ƽ��������У�
B�����п��Կ����Ǽ���ʼ���ﵽƽ��״̬���ټ���0.1molNO��0.1molCO���൱������ƽ��ѹǿ��ƽ��������У�
C����״̬��ƽ��ʱCO2���ʵ���Ϊ0.10mol��������м������ƽ�ⳣ����������ʼ������Ũ���̺�ƽ�ⳣ���Ƚ��жϷ�Ӧ���з���
D��T2��ʱ������ͼ���֪ƽ��״̬��CO2���ʵ���Ϊ0.12mol������ʼʱ����г���0.06mol N2��0.12 mol CO2����Ӧ������еõ�ƽ��״̬������ʼ��Ϊ0.12molNO��0.12molCO�ﵽ��ƽ���Ч������ʼ��0.2molCO��0.2molNO��ȣ��൱�ڼ�����NO��CO��0.08mol���൱��ѹǿ��Сƽ��������У�
��� �⣺A.2NO��g��+2CO��g��?N2��g��+2CO2��g�����ȹ���ƽ�¶ȸߣ���״̬�¶ȸ��ڱ���T1��T2����ʱ��ƽ��״̬������̼���ʵ���С��˵���¶�Խ��ƽ��������У��淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ����A����
B�����п��Կ����Ǽ���ʼ���ﵽƽ��״̬���ټ���0.1molNO��0.1molCO���൱������ƽ��ѹǿ��ƽ��������У��ﵽƽ��ʱ������CO2����������ȼ��еĴ�B����
C����״̬��ƽ��ʱCO2���ʵ���Ϊ0.10mol��������м������ƽ�ⳣ����
2NO��g��+2CO��g��?N2��g��+2CO2��g��
��ʼ����mol/L�� 0.1 0.1 0 0
�仯����mol/L�� 0.05 0.05 0.025 0.05
ƽ������mol/L�� 0.05 0.05 0.025 0.05
K=$\frac{0.05{\;}^{2}��0.025}{0.05{\;}^{2}��0.05{\;}^{2}}$=10��
T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2��Qc=$\frac{0.20{\;}^{2}��0.20}{0.20{\;}^{2}��0.20{\;}^{2}}$=5��K=10����Ӧ�ﵽ��ƽ��ǰv��������v���棩����C����
D��T2��ʱ��ƽ��״̬CO2���ʵ���Ϊ0.12mol��
2NO��g��+2CO��g��?N2��g��+2CO2��g��
��ʼ����mol�� 0.2 0.2 0 0
�仯����mol�� 0.12 0.12 0.06 0.12
ƽ������mol�� 0.08 0.08 0.06 0.12
2NO��g��+2CO��g��?N2��g��+2CO2��g��
��ʼ����mol�� 0 0 0.06 0.12
ת���� 0.12 0.12 0 0
����ʼʱ����г���0.06mol N2��0.12 mol CO2����Ӧ������еõ�ƽ��״̬������ʼ��Ϊ0.12molNO��0.12molCO�ﵽ��ƽ���Ч�������ٺ���ʼ��0.2molCO��0.2molNO��ȣ��൱�ڼ�����NO��CO��0.08mol��ѹǿ��Сƽ��������У����Ե���ת���ʴ���40%����D��ȷ��
��ѡD��
���� ���⿼���˻�ѧƽ��Ӱ�����أ����ݷ����жϣ���Ҫ��ƽ�ⳣ���ļ����ͼ�ߵ�����Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | |
| B�� | ʯ������ϡ���ᷴӦ��H++OH-�TH2O | |
| C�� | ������þ�������Mg��OH��2+2H+�TMg2++2H2O | |
| D�� | ͭƬ������������Һ�У�Cu+Ag+�TCu2++Ag |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
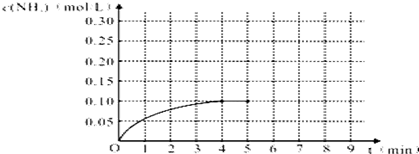
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
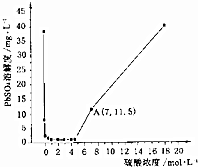 ��֪25��ʱKSP��PbSO4��=1.6��10-8��KSP��BaSO4��=1.1��10-10�����¶���PbSO4�ڲ�ͬŨ�ȵ������е��ܽ����ͼ��ʾ�������й�˵������ȷ���ǣ�������
��֪25��ʱKSP��PbSO4��=1.6��10-8��KSP��BaSO4��=1.1��10-10�����¶���PbSO4�ڲ�ͬŨ�ȵ������е��ܽ����ͼ��ʾ�������й�˵������ȷ���ǣ�������| A�� | ͼ��A��c��SO42-��=7mol•L-1 | |
| B�� | ���˵�PbSO4��������ϡ����ϴ�ӣ����Լ��ٳ������ | |
| C�� | ����Ũ�ȴ���5mol•L-1ʱ��PbSO4�ܽ�������ԭ����ת����Pb��HSO4��2 | |
| D�� | ��Pb��NO3��2��Ba��NO3��2�����Һ����ϡ�����У�������PbSO4��BaSO4���ֳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
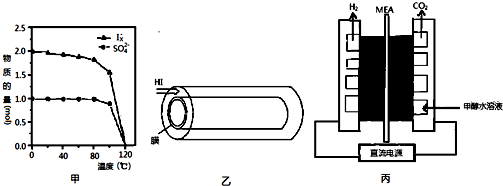
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ϩ��
����ϩ��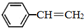 ���������������ϵ���Ҫ���壬��ͨ���ұ��������Ƶã�
���������������ϵ���Ҫ���壬��ͨ���ұ��������Ƶã� CH2CH3��g��$\stackrel{����}{?}$
CH2CH3��g��$\stackrel{����}{?}$ =CH2��g��+H2��g����=-Q1kJ��mol-1
=CH2��g��+H2��g����=-Q1kJ��mol-1 ��
��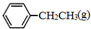 ��
�� ��H2��g����ȼ���ȣ���H���ֱ�Ϊ-Q1 kJ•mol-1��-Q2kJ•mol-1��-Q3 kJ•mol-1��д��Q��Q1��Q2��Q3�Ĺ�ϵʽQ2+Q3-Q1��
��H2��g����ȼ���ȣ���H���ֱ�Ϊ-Q1 kJ•mol-1��-Q2kJ•mol-1��-Q3 kJ•mol-1��д��Q��Q1��Q2��Q3�Ĺ�ϵʽQ2+Q3-Q1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
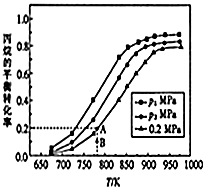 ��ϩ��C3H6��������۱�ϩ����ϩ��Ȼ�����Ʒ��ԭ�ϣ�Ŀǰ���ڿ������飨C3H8���ѽ���ȡ��ϩ����ԭ��ΪC3H8��g��?C3H6��g��+H2��g����H���ش��������⣺
��ϩ��C3H6��������۱�ϩ����ϩ��Ȼ�����Ʒ��ԭ�ϣ�Ŀǰ���ڿ������飨C3H8���ѽ���ȡ��ϩ����ԭ��ΪC3H8��g��?C3H6��g��+H2��g����H���ش��������⣺| ���ۼ� | C-C | C=C | C-H | H-H |
| ����/KJ•mol-1 | 348 | 615 | 413 | 436 |
| n��CO2��/n��C3H8���¶�/K | 600 | 700 | 800 | 900 | 1000 |
| 0��1 | 1.0% | 6.3% | 24.4% | 59.6% | 87.0% |
| 1��1 | 2.7% | 12.9% | 41.6% | 78.0% | 94.5% |
| 1��2 | 3.7% | 17.2% | 50.9% | 85.3% | 97.1% |
| 1��3 | 4.0% | 20.5% | 57.7% | 89.5% | 98.2% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ö��Ե缫���1L1mol•L-1��CuSO4��Һ������������3.2gͭʱ������0.05molCu��OH��2����ɽ���Һ�ָ���ԭŨ�� | |
| B�� | Hg��l��+H2SO4��aq���THgSO4��aq��+H2��g�������²����Է����У�˵����H��0 | |
| C�� | ��֪25��ʱ��Ksp��AgCl��=1.8��10-10��Ksp��Ag2CrO4��=2.0��10-12������AgCl���ܽ�ȴ���Ag2CrO4���ܽ�� | |
| D�� | 25��ʱ����0.1 mol•L-1 CH3COOH��Һ�м�������CH3COONa���壬����Һ��ˮ�ĵ���̶Ƚ�������Kw���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�5.6 L���Ȼ�̼���еķ�����Ϊ0.25NA | |
| B�� | ��״���£�14 g������11.2LNH3���е�ԭ������ͬ | |
| C�� | ��״���£�22.4 L����ȵ������������Ļ�������к��еķ���������ΪNA | |
| D�� | ���ʵ���Ũ��Ϊ0.5mol/L MgCl2��Һ������Cl-������Ϊ1NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com