



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������£�11.2 L������ȫ����1 Lˮ�У�������Һ��Cl-��ClO-����������֮��ΪNA |
| B���ܱ������У�0.1 mol H2��25.4 g����һ�������³�ַ�Ӧ������HI������Ϊ0.2 NA |
| C������4 NA��̼̼�Ҽ��Ľ��ʯ��������Ϊ24 g |
| D����0.1 mol FeCl3����Һ��ȫˮ���õ��Ľ������Ӹ���Ϊ0.1 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1 mol/L | B��0.2 mol/L |
| C��0.3 mol/L | D��0.4 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��18 g H2O�к��е�������Ϊ10NA |
| B��12 g���ʯ�к��еĹ��ۼ���Ϊ4NA |
| C��46 g NO2��N2O4��������к���ԭ������Ϊ3NA |
| D��1 mol Na������O2��Ӧ������Na2O��Na2O2�Ļ�����ʧȥNA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
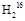 O��80 g
O��80 g  O�����ʵ���֮����������,����������������֮��������������,����������֮������������,���Ƿֱ���Na��Ӧʱ,���ų��������֮��(ͬ����)��������������,����֮������������������
O�����ʵ���֮����������,����������������֮��������������,����������֮������������,���Ƿֱ���Na��Ӧʱ,���ų��������֮��(ͬ����)��������������,����֮������������������ �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NA��N2������0.5 NA��H2������ռ�������һ����2 : 1 |
| B����ͬ���ʵ�����OH����CH3+������ͬ��Ŀ�ĵ��� |
| C��25��ʱ��pH��13��Ba(OH)2��Һ�к���OH������ĿΪ0.2NA |
| D�����³�ѹ�£�NO2������H2O��Ӧ����0.1molNO����ת�Ƶĵ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c1��2c2 | B��c2<2c1 |
| C��c2>2c1 | D��c2��2c1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com