
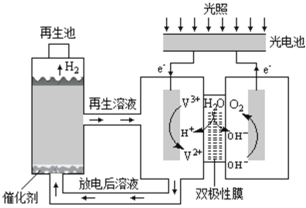
【题目】利用光能分解水的装置如图,在直流电场作用下,双极性膜将水解离为H+和OH,并实现其定向通过。下列说法错误的是( )
A.光电池能将光能转化为电能
B.阳极区发生的电极反应为:2H2O4e=4H++O2↑
C.双极性膜能控制两侧溶液的酸碱性不同
D.再生池中发生的反应为:2V2++2H+=2V3++H2↑
【答案】B
【解析】
由图上电子的移动方向可知右侧电解池的阳极,反应式为4OH--4e-=2H2O+O2↑,左侧为阴极,反应式为2V3++2e-=2V2+;双极性膜可将水解离为H+和OH-,由图可知,H+进入阴极,OH-进入阳极,放电后的溶液进入再生池中在催化剂条件下发生反应放出氢气,反应方程式为2V2++2H+=2V3++H2↑,由此来解题。
A.由图可知,该装置将光能转化为化学能并分解水,选项A正确;
B.光照过程中阳极区发生的电极反应为:4OH--4e-=2H2O+O2↑,选项B错误;
C.双极性膜可将水解离为H+和OH-,由图可知,H+进入阴极,OH- 进入阳极,则双极性膜可控制其两侧溶液分别为酸性和碱性,选项C正确;
D.根据以上分析,再生的反应方程式为2V2++2H+=2V3++H2↑,选项D正确;
答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】300℃下,在一容积为2 L的恒容密闭容器中加入0.2 mol CO和0.4 mol H2,发生如下反应:CO(g)+2H2(g) ![]() CH3OH(g) 。下列各物理量随反应时间变化趋势的曲线不正确的是
CH3OH(g) 。下列各物理量随反应时间变化趋势的曲线不正确的是
A. 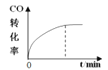 B.
B. 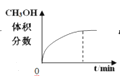
C. 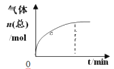 D.
D. 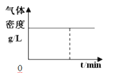
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H2-△H1=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)能判断CO2(g)+H2(g)![]() CO(g)+H2O(g)达到化学平衡状态的依据是____(填字母)。
CO(g)+H2O(g)达到化学平衡状态的依据是____(填字母)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。

该条件下反应的平衡常数为_____;若铁粉足量,CO2的起始浓度为2.0mol·L-1,则平衡时CO的浓度为____mol·L-1。
②下列措施中能使平衡时![]() 增大的是___(填字母)。
增大的是___(填字母)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的还原产物,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题:
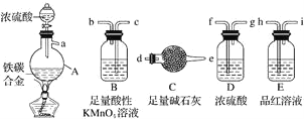
(1)该装置的连接顺序a___(填接口字母),连接好装置后,首先应进行的操作是____。
(2)mg铁碳合金中加入浓H2SO4,点燃酒精灯一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:A:只含有Fe3+;B:只含有Fe2+;C:____,若为A,则A中反应的化学方程式为___,验证C种可能的实验方法___。
(3)待A中不再逸出气体时,停止加热,拆下C并称重,C增重bg。铁碳合金中铁的质量分数____(写表达式)。
(4)某同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:_____。
(5)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 对此聚合物分析正确的是( )
对此聚合物分析正确的是( )
A. 其单体是CH2=CH2和HCOOC2H5
B. 它是缩聚反应产物
C. 其单体是CH2=CH-COOC2H5
D. 其链节是CH3CH2-COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是( )

A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下氨气能与 CaCl2 固体结合生成 CaCl2·8NH3。下列说法不正确的是
A.CaCl2·6NH3(s)+ 2NH3(g) ![]() CaCl2·8NH3(s) ΔH < 0
CaCl2·8NH3(s) ΔH < 0
B.实验室可用氯化铵固体和熟石灰共热来制备氨气,说明相对高温不利于 CaCl2 与氨气的化合
C.常温下,在密闭容器中缩体加压能增加体系中活化分子百分数,有利于氨气的吸收
D.CaCl2·6NH3(s) CaCl2·c4NH3(s)+ 2NH3(g),He 气流可促进反应进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项中所示的物质间转化均能实现的是( )
A.Al(s)![]() Al(OH)3(s)
Al(OH)3(s)![]() Al2O3(s)
Al2O3(s)
B.FeS2(s)![]() SO2(g)
SO2(g)![]() BaSO3(s)
BaSO3(s)
C.Cl2(g)![]() NaClO(aq)
NaClO(aq)![]() HClO(aq)
HClO(aq)
D.Fe(s)![]() Fe2O3(s)
Fe2O3(s)![]() Fe2(SO4)3(aq)
Fe2(SO4)3(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com