
【题目】合成尿素的反应为:2NH3(g)+CO2(g) ![]() CO(NH2)2(s)+H2O(g) △H<0。一定条件下,在10 L的恒容密闭容器中,充入2 mol NH3和1 mol CO2,反应经5 min后达 到平衡,测得容器中CO2的浓度为0.05molL-1 。
CO(NH2)2(s)+H2O(g) △H<0。一定条件下,在10 L的恒容密闭容器中,充入2 mol NH3和1 mol CO2,反应经5 min后达 到平衡,测得容器中CO2的浓度为0.05molL-1 。
完成下列填空:
(1)平均反应速率υ(NH3)=____________。
(2)下列描述中能说明上述反应已达平衡的是_________。(填序号)
a.气体的平均相对分子质量不随时间而变化 b.NH3和CO2的比例保持不变
c.气体的压强不再发生变化 d.2υ正(NH3)=υ逆(H2O)
(3)为提高尿素的产率,工业上用该反应生产尿素时,合适的反应条件是_______。(填序号)
a.24000kPa b.200℃ c.800℃ d.101 kPa
【答案】0.02 molL-1min-1 ac a b
【解析】
(1)根据已知信息,计算平衡时氨气的转化量,再根据公式![]() 计算速率;
计算速率;
(2)根据化学平衡状态的特征判断,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3)根据影响平衡移动的因素进行分析。
(1)一定条件下,在10L的恒容密闭容器中,充入2mol NH3和1mol CO2,反应经5min后达到平衡,测得容器中CO2的浓度为0.05mol·L-1,则消耗0.5molCO2、1molNH3,则氨气的反应速率为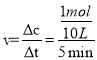 =0.02molL-1min-1;
=0.02molL-1min-1;
(2)a.反应前后气体的物质的量不等,气体的平均相对分子质量不随时间而变化,可说明达到平衡状态,故a正确;
b.充入2mol NH3和1mol CO2,且按2:1反应,则无论是否达到平衡状态,NH3和CO2的比例都保持不变,故b错误;
c.反应前后气体体积不等,则气体的压强不再发生变化,可说明达到平衡状态,故c正确;
d.2υ正(NH3)=υ逆(H2O),正逆反应速率不等,没有达到平衡状态,故d错误;
故选:ac;
(3)为提高氨气的转化率,采用使得化学平衡正向移动的措施即可,工业上用该反应生产尿素时,合适的反应条件是高温高压,
故选:a b。


科目:高中化学 来源: 题型:
【题目】某烃与氢气发生反应后能生成(CH3)2CHCH2CH3,则该烃不可能是
A. 2-甲基-2-丁烯 B. 3-甲基-1-丁烯
C. 2.3-二甲基-1-丁烯 D. 3-甲基-1-丁炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-溴丙烷是一种重要的有机合成中间体。实验室制备少量1-溴丙烷的主要步骤如下:

步骤1:在仪器A中加入搅拌磁子、12g 1-丙醇及20mL水,在冰水冷却下缓慢加入28mL浓H2SO4;冷却至室温,搅拌下加入24g NaBr。
步骤2:缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分离出有机相。
步骤4:将分离出的有机相转入分液漏斗,依次用H2O、5%的Na2CO3溶液洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
已知:①1-溴丙烷沸点为71℃,密度为1.36g/cm3;
②反应过程中,在仪器A中可以观察到A的上方出现红棕色蒸气(Br2)。
回答下列问题:
(1)仪器A的名称是______;加入搅拌磁子的目的是搅拌和______。
(2)仪器A中主要发生反应为:NaBr + H2SO4===HBr + NaHSO4和______。
(3)步骤2中需向接收瓶内加入少量冰水并置于冰水浴中的目的是______,同时可以观察到的现象是______。
(4)步骤4中的两次洗涤,依次洗去的主要杂质是______、_________。
(5)步骤4中的Na2CO3溶液还可以用下列中的______试剂代替。
A.NaOH溶液 B.NaI溶液 C.Na2SO3溶液 D.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,发生可逆反应A(s)+2B(g)![]() 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 molC和2 molD加入乙容器中。起始时,两容器中的压强相等,t1时两容器内均达到平衡状态(如图所示,隔板K固定不动)。下列说法正确的是( )
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 molC和2 molD加入乙容器中。起始时,两容器中的压强相等,t1时两容器内均达到平衡状态(如图所示,隔板K固定不动)。下列说法正确的是( )
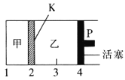
A.向甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度与乙中C的浓度相等
B.t1时,甲、乙两容器中的压强仍相等
C.移动活塞P,使乙的容积和甲的相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.分别向甲、乙中加入等量的氦气,甲中反应速率和乙中的反应速率均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图装置(气密性好)研究钠与氯气的反应。

实验步骤:
①将一定量浓盐酸滴在KMnO4粉末上,立即产生黄绿色气体。
②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。
(1)步骤①,黄绿色气体是氯气,则KMnO4的作用是__________(填“氧化剂”或“还原剂”)。
(2)步骤③,引起钠燃烧的原因是____________。
(3)生成白色固体的化学方程式是______________。
(4)结合离子方程式说明NaOH溶液的作用是_______________。
(5)实验结束后,甲同学在安全、环保的理念指导下,仅用上图装置就完成了集气瓶内残余氯气的处理,其操作是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬铁矿主要含有亚铬酸亚铁![]() ,还含有少量
,还含有少量![]() 和
和![]() 。由铬铁矿制备
。由铬铁矿制备![]() 的流程如图1所示:
的流程如图1所示:

已知:常温下,![]() ,
,![]() 。
。
回答下列问题:
(1)铬铁矿与![]() 、
、![]() 混合煅烧之前应先将其粉碎,目的是_______________。
混合煅烧之前应先将其粉碎,目的是_______________。
(2) “煅烧”过程中主要反应的化学方程式为_______![]() _______
_______![]() _______
_______![]() _______
_______![]() _______
_______![]() _______
_______![]() _______
_______![]() 。
。
(3)已知:![]() 和
和![]() 与
与![]() 高温煅烧可生成
高温煅烧可生成![]() 和
和![]() 。“滤渣1”的主要成分为_____________________
。“滤渣1”的主要成分为_____________________![]() 填化学式
填化学式![]() ,其一种用途为_____________________
,其一种用途为_____________________
(4)“调pH”的过程即是用酸酸化使pH约为5,其目的是_____________________,“滤渣2”的主要成分为_____________________![]() 填化学式
填化学式![]() ,同时
,同时![]() 转化为
转化为![]() ,此转化过程的离子方程式为____________________________。
,此转化过程的离子方程式为____________________________。
(5)![]() 、KCl、
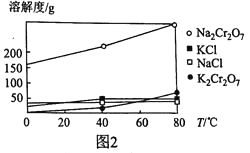
、KCl、![]() 、NaCl的溶解度曲线如图2所示,结合图象解释向
、NaCl的溶解度曲线如图2所示,结合图象解释向![]() 溶液中加入KCl固体经一系列操作后得到
溶液中加入KCl固体经一系列操作后得到![]() 的理由:_____________________________。
的理由:_____________________________。
(6)该流程产生的含铬废水不能随意排放,可通过电解法处理![]() 装置如图3所示
装置如图3所示![]() ,电解时,在阴极区可生成
,电解时,在阴极区可生成![]() 和
和![]() 沉淀,电解后溶液中
沉淀,电解后溶液中![]() ,则溶液中
,则溶液中![]() ____________
____________![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种有机物,它们有如下相互转化关系:

已知:A是相对分子质量为28的烃,E属于高分子化合物。请完成下列各题:
(1)物质A的名称是______________,物质D的结构简式为____________________。
(2)写出反应①的化学方程式:_______,该反应属于_____________反应。
(3)写出反应②的化学方程式:______________,该反应属于_____________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银制器皿表面日久因生成Ag2S而变黑,可进行如下处理:将表面发黑的银器浸入盛有食盐水的铝质容器中(如图),一段时间后黑色褪去。有关说法正确的是( )

A.该处理过程中电能转化为化学能
B.银器为正极,Ag2S还原为单质银
C.Ag2S溶解于食盐水生成了AgCl
D.铝质容器质量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。

回答下列问题:
(1)图B对应的物质名称是_________,其晶胞中的原子数为______,晶体类型为_______。
(2)d中元素的原子核外电子排布式为_______。
(3)图A中由二种元素组成的物质中,沸点最高的是______,原因是______,该物质的分子构型为_________,中心原子的杂化轨道类型为_________。
(4)图A中的双原子分子中,极性最大的分子是_________。
(5)k的分子式为_________,中心原子的杂化轨道类型为_________,属于_________分子(填“极性”或“非极性”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com