
| 实验次序 | 温度(℃) | 冷却后剩余固体的质量(g) |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
| 90 |
| 250 |
| m |
| M |
| 90 |
| 250 |
| 0.576g |
| 18g/mol |
| 5.12g |
| 160g/mol |
| 0.032mol |
| 0.5mol/L |


 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
A、硝基苯的结构简式为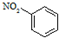 |
B、表示甲烷分子或四氯化碳分子的比例模型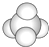 |
| C、等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 |
D、结构片段为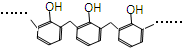 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:
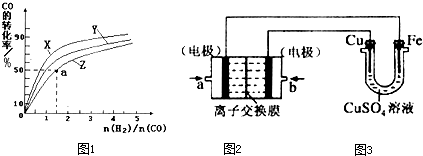
查看答案和解析>>
科目:高中化学 来源: 题型:
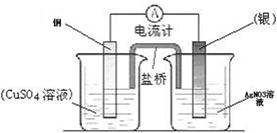 依据某氧化还原反应设计的原电池如图所示.
依据某氧化还原反应设计的原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 颜色 | Ksp | |
| AgCl | 白色 | 1.8×10-10 mol2?L-2 |
| AgBr | 浅黄色 | 5.0×10-13 mol2?L-2 |
| AgI | 黄色 | 8.3×10-17 mol2?L-2 |
| Ag2CrO4 | 砖红色 | 1.1×10-12 mol3?L-3 |
| HgS | 黑色 | 1.6X10-52 mol2?L-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3溶液的水解:CO32-+H3O+?HCO3-+H2O |
| B、AlCl3溶液中滴加浓氨水至过量:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| C、氯化亚铁溶液中加入硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
| D、向NaHSO4溶液中加入过量Ba(OH)2溶液:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | HX | HY | HZ | ||
| 浓度mol/L | 0.1 | 0.5 | 0.9 | 1 | 1 |
| 电离度% | 0.3 | 0.15 | 0.1 | 0.3 | 10 |
| A、HX>HY>HZ |
| B、HZ>HX>HY |
| C、HY>HZ>HX |
| D、HZ>HY>HX |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com