
在一密闭容器中进行如下反应:2SO2(气)+O2(气) 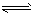 2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
A.SO2为0.4mol/L、O2为0.2mol/L B.SO2为0.25mol/L
C.SO2、SO3均为0.15mol/L D.SO3为0.4mol/L
科目:高中化学 来源:2016-2017学年天津市高二12月月考化学卷(解析版) 题型:选择题
已知反应:①101kPa时,2C(石墨)+ O2(g)= 2CO(g) ΔH= -221 kJ/mol
②稀溶液中,H +(aq)+ OH-(aq)= H2O(1) ΔH= -57.3 kJ/mol
下列结论正确的是
A.C(石墨)的燃烧热大于 110.5 kJ/mol
B.稀硫酸与稀 NaOH溶液反应的反应热为-57.3 kJ/mol
C.若已知CO的燃烧热为283kJ/mol,则C(金刚石)的燃烧热为393.5 kJ/mol
D.稀醋酸与稀 NaOH溶液反应,每生成 1mol液态水就会放出 57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安一中高二上月考二化学卷(解析版) 题型:选择题
某金属能与盐酸反应放出氢气,该金属与锌组成的原电池中,锌为原电池的负极,则金属可能是
A.铝 B.铜 C.铁 D.镁
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上月考四化学卷(解析版) 题型:填空题
(1)已知常温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,则该溶液的pH= ,此酸的电离平衡常数K= ,由HA电离出的H+的浓度约为水电离出的H+的浓度的 倍。
(2)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶剂。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①向该溶液中加入少量盐酸时,发生反应的离子方程式是 ,向其中加入少量KOH溶液时,发生反应的离子方程式是 。
②现将0.04mol﹒L-1HA溶液和0.02mol﹒L-1NaOH溶液等体积混合,得到缓冲溶液。
a、若HA为HCN,该溶液显碱性,则溶液中c(Na+) c(CN-)(填“<”、“=”或“>”)。
b、若HA为CH3COOH,该溶液显酸性,溶液中所有的离子按浓度由大到小排列的顺序是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上月考四化学卷(解析版) 题型:选择题
可以将反应Zn+Br2=ZnBr2设计成蓄电池,下列4个电极反应
①Br2+2e-=2Br-
②2Br--2e-=Br2
③Zn-2e-=Zn2+
④Zn2++2e-=Zn
其中表示充电时的阳极反应和放电时的负极反应的分别是
A.②和③ B.②和① C.③和① D.④和①
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上月考四化学卷(解析版) 题型:选择题
下列说法正确的是
A.可逆反应的特征是正反应速率和逆反应速率相等
B.在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态
C.在其他条件不变时,升高温度可以使化学平衡向吸热反应方向移动
D.在其他条件不变时,增大压强一定会破坏气体反应的平衡状态
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一12月月考化学卷(解析版) 题型:推断题
A、B、C、X是中学化学中常见的物质,它们之间的转化关系加下图所示(部分产物已略去)。请回答下列问题:

(1)若A能使湿润的红色石蕊试纸变蓝,C为红棕色的气体。A转化为B的化学方程为 ,
请写出实验室制取A的化学方程式: 。
(2)若B是一种常见的温室气体,则B转化为C的化学方程式 。
(3)若X是金属单质,向B、C溶液中分别滴加AgNO3溶液,均产生不溶于稀硝酸的白色沉淀,则B的化学式为 。保存C溶液常加入少量X,其目的是 ,请写出B转化为C的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一12月月考化学卷(解析版) 题型:选择题
下列关于氧化还原反应的叙述,正确的是
A.有一种元素得电子,肯定有另一种元素失电子
B.在反应中不一定所有元素的化合价都发生变化
C.某元素由化合态变为游离态,则该元素一定得电子
D.氧化还原反应中不一定有电子的转移
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二12月月考化学卷(解析版) 题型:选择题
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是
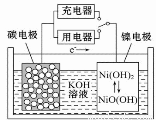
A.充电时,阴极的电极反应为:Ni(OH)2+OH--e-===NiO(OH)+H2O
B.放电时,负极的电极反应为:H2- 2e-+2OH-=== 2H2O
2e-+2OH-=== 2H2O
C.放电时,OH-移向镍电极
D.充电时,将电池的碳电极与外电源的正极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com