
实验探究是体验知识的产生或形成过程的基本途径.下面是某同学探究实验报告的一部分,请填空:
实验名称:氯、溴、碘的氧化性强弱比较
实验药品:NaCl溶液、KBr溶液、KI溶液、氯水、溴水、四氯化碳
实验步骤 实验结论
①NaCl溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 氧化性从强到弱的顺序:氯、溴、碘
②KBr溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色
③KI溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色
(1)完成该实验需用到的仪器是 ;
(2)CCl4在实验中所起的作用是 ;
(3)在实验②中四氯化碳层颜色变化过程为由 ;
(4)该同学的实验缺陷是 .
考点: 卤素原子结构及其性质的比较.
专题: 卤族元素.
分析: (1)该实验用量筒量取试剂,可在试管中进行反应;
(2)四氯化碳不参加反应,但卤素单质不易溶于水,易溶于四氯化碳;
(3)实验②中四氯化碳溶解生成的溴,在下层;
(4)不能比较溴、碘的氧化性强弱,以此来解答.
解答: 解:由非金属单质间的置换反应来比较单质的氧化性强弱可知,Cl2能置换出Br2、I2,Br2能置换出I2,则说明氧化性Cl2>Br2>I2,
(1)该实验用量筒量取试剂,可在试管中进行反应,还需要胶头滴管滴加液体,故答案为:试管、量筒、胶头滴管;
(2)四氯化碳不参加反应,但卤素单质不易溶于水,易溶于四氯化碳,所以其作用为萃取剂,使生成的Br2、I2溶于其中,便于观察现象,
故答案为:萃取剂,使生成的Br2、I2溶于其中,便于观察现象;
(3)实验②中四氯化碳溶解生成的溴,在下层,则观察到四氯化碳层颜色变化过程为由无色逐渐变为红棕色,
故答案为:由无色逐渐变为红棕色;
(4)设计的实验中不能证明溴的氧化性强于碘,应再做一组实验④,步骤为:KI溶液+溴水+1mL CCl4,振荡,静置,观察CCl4层颜色,
故答案为:不能证明溴的氧化性强于碘;再做一组实验④,步骤为:KI溶液+溴水+1mL CCl4,振荡,静置,观察CCl4层颜色.
点评: 本题考查卤素单质之间的置换反应的实验设计,把握单质的氧化性强弱及现象的分析为解答的关键,涉及氧化还原反应氧化性的比较及萃取等知识点,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在.有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:
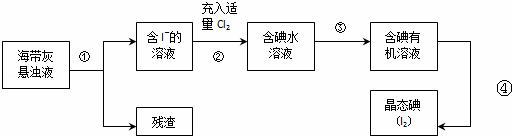
(1)步骤①需要用到的玻璃仪器(除烧杯外)还有
(2)指出提取碘的过程中有关的实验操作名称:③ .
查看答案和解析>>
科目:高中化学 来源: 题型:
完成并配平下列方程式(在横线上填写化学计量数,在方框内填写化学式):
Fe(OH)3+ +3KClO﹣ K2FeO4+ KCl+ H2O
(2)用一种试剂除去BaCl2溶液中含有的HCl,写出所用试剂及离子方程式.除杂试剂: .离子方程式
(3)鉴别饱和碳酸氢溶液和BaCl2溶液,可选用鉴别的试剂有(填编号) .
A.盐酸B.碳酸钠溶液C.澄清石灰水D.氨水
依次写出鉴别中有明显现象的反应的离子方程式 ;
少量澄清石灰水:
或过量澄清石灰水: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是()
A. 在共价化合物中不可能含有离子键
B. 非金属之间形成的化学键一定是共价键
C. 含有共价键的化合物不一定是共价化合物
D. 含有离子键的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:2Ag+Zn(OH)2 Ag2O+Zn+H2O,在此电池放电时,负极上发生反应的物质是()
Ag2O+Zn+H2O,在此电池放电时,负极上发生反应的物质是()
A. Ag B. Zn(OH)2 C. Ag2O D. Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
硅是一种重要的非金属单质,其化学性质与碳既有相似之处,也有不同之处.在常温下,下列物质能够与硅发生反应的是()
A. HF B. HNO3 C. NaCl D. H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要配制2mol/l的NaCl溶液450ml,配制时应选用的容量瓶的规格和称取的NaCl质量分别是()
A. 450ml,52.65g B. 任意规格,52.65g
C. 500 ml,58.5g D. 1000 ml,117g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com