
| A. | 金属钠投入CuSO4溶液中:2Na+Cu2+═2Na++Cu | |
| B. | 过量的CO2通入Ca(ClO)2溶液中:ClO-+CO2+H2O═HCO3-+HClO | |
| C. | 向Mg(OH)2悬浊液中滴加四滴0.1mol•L-1FeCl3溶液:3Mg(OH)2(S)+2Fe3+(aq)═2Fe(OH)3(S)+3Mg2+(aq) | |
| D. | 铅酸蓄电池充电时的阳极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
分析 A.不符合反应客观事实;
B.二氧化碳过量反应生成次氯酸和碳酸氢钙;
C.氢氧化铁溶解性弱于氢氧化镁,实现沉淀的转化;
D.铅酸蓄电池充电时的阳极发生氧化反应,硫酸铅失去电子生成二氧化铅和硫酸;
解答 解:A.金属钠投入CuSO4溶液中,离子方程式:2H2O+2Na+Cu2+═2Na++Cu(OH)2↓+H2↑,故A错误;
B.过量的CO2通入Ca(ClO)2溶液中,离子方程式:ClO-+CO2+H2O═HCO3-+HClO,故B正确;
C.向Mg(OH)2悬浊液中滴加四滴0.1mol•L-1FeCl3溶液,离子方程式:3Mg(OH)2(S)+2Fe3+(aq)═2Fe(OH)3(S)+3Mg2+(aq),故C正确;
D.铅酸蓄电池充电时的阳极反应,离子方程式:PbSO4+2H2O-2e-═PbO2+4H++SO42-,故D正确;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应遵循客观事实,遵循原子个数、电荷守恒规律,题目难度中等.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:实验题
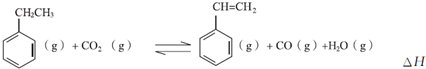
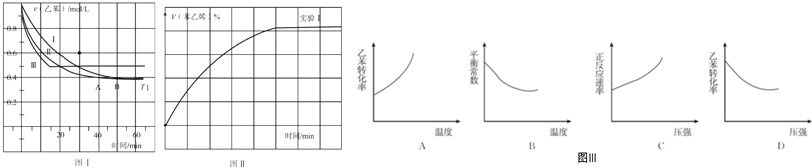

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 向NaAlO2溶液中持续通入气体Y | 先出现白色沉淀,最终沉淀又溶解 | Y可能是SO3气体 |
| B | 向某溶液中加入Cu 和浓H2SO4 | 试管口有红棕色气体产生 | 原溶液可能含有NO3- |
| C | 将Na投到一定浓度的CuCl2溶液 | 出现气泡并有固体生成 | Na与CuCl2溶液反应,有H2和Cu生成 |
| D | 向浓度均为0.1mol/L的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3是某些胃药的一种成分 | |
| B. | 乳酸铁是某些补铁口服液的有效成分 | |
| C. | 臭氧可以作为新型自来水消毒剂 | |
| D. | SO2常用作红葡萄酒中杀菌消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CO、2mol H2 | 1mol CH3OH | 2mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2c1>c3 | B. | a+b=90.7 | C. | 2V2<V3 | D. | α1+α3=0.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅酸可使紫色石蕊试液变红色 | |
| B. | 二氧化硫通入紫色石蕊试液中.试液先变红后褪色 | |
| C. | 可用锌粒与稀硝酸反应制备氢气 | |
| D. | 液溴易挥发,所以存放液溴的试剂瓶中应加水封保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
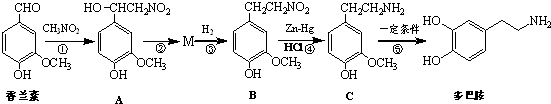
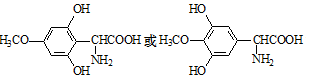 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com