
【题目】晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用过量的碳还原二氧化硅制得粗硅,同时得到一种可燃性气体;
② 粗硅与干燥的HCl气体反应制得SiCl3(Si+ 3HCl![]() SiCl3 + H2)
SiCl3 + H2)
③ SiHC13与过量的H2在1100~1200℃的温度下反应制得纯硅,已知SiHCi3。能与水剧烈反应,在空气中易自燃。
请回答:
(1)第一步制取粗硅的化学反应方程式为_________。
(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃ )中含有少量SiC14 (沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHC13采用的方法为________。
(3)实验室用SiHCl3 与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):

①装置B中的试剂是___________,装置C中的烧杯需要加热,目的是___________。
②反应一段时间后,装置D中观察到的现象是___________,装置D不能采用普通玻璃管的原因是___________,装置D中发生反应的化学方程式是___________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及___________。
【答案】(1)SiO2+2C![]() Si+ 2CO↑ ;(2)分馏(或蒸馏);
Si+ 2CO↑ ;(2)分馏(或蒸馏);
(3)①浓硫酸;使滴入烧瓶中的SiHC13汽化;
②有固体物质生成 ;在题给反应温度下(1100~ 1200℃ ),普通的玻璃会软化;
SiHCl3+H2![]() Si+3HCl
Si+3HCl
③排尽装置中的空气。
【解析】
试题分析:(1)高温下用碳还原二氧化硅生成硅与一氧化碳,反应方程式为SiO2+2C![]() Si+ 2CO↑;(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃ )中含有少量SiC14 (沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHC13采用的方法为,应用二者的沸点相差较大,所以提纯SiHCl3的方法只能在无水的条件下利用它们的沸点不同,采用分馏的方法进行,采用蒸馏的方法;(3)①装置A中产生氢气,由于氢气中含有水蒸汽,所以装置B中的试剂是浓硫酸,利用浓硫酸的吸水性对氢气进行干燥处理,装置C中的烧杯需要加热,目的是使滴入烧瓶中的SiHC13汽化;②在装置D中氢气与SiHC13发生反应产生Si单质和HCl,所以反应一段时间后,装置D中观察到的现象是有固体物质生成;装置D不能采用普通玻璃管的原因是在题给反应温度下(1100~ 1200℃ ),普通的玻璃会软化,不能进一步发生反应;装置D中发生反应的化学方程式是SiHCl3+H2
Si+ 2CO↑;(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃ )中含有少量SiC14 (沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHC13采用的方法为,应用二者的沸点相差较大,所以提纯SiHCl3的方法只能在无水的条件下利用它们的沸点不同,采用分馏的方法进行,采用蒸馏的方法;(3)①装置A中产生氢气,由于氢气中含有水蒸汽,所以装置B中的试剂是浓硫酸,利用浓硫酸的吸水性对氢气进行干燥处理,装置C中的烧杯需要加热,目的是使滴入烧瓶中的SiHC13汽化;②在装置D中氢气与SiHC13发生反应产生Si单质和HCl,所以反应一段时间后,装置D中观察到的现象是有固体物质生成;装置D不能采用普通玻璃管的原因是在题给反应温度下(1100~ 1200℃ ),普通的玻璃会软化,不能进一步发生反应;装置D中发生反应的化学方程式是SiHCl3+H2![]() Si+3HCl;③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及排尽装置中的空气,防止氢气与氧气混合发生爆炸,同时也可以防止产生的Si单质被氧化。
Si+3HCl;③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及排尽装置中的空气,防止氢气与氧气混合发生爆炸,同时也可以防止产生的Si单质被氧化。


科目:高中化学 来源: 题型:
【题目】为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )

A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题:
(1)用离子方程式表示盐碱地(含较多Na2CO3)呈碱性的原因:____________;相同浓度的Na2CO3溶液与NaHCO3溶液等体积混合后,溶液中c(HCO3-) ____c(CO32-)(用“>、<、=”表示)。
(2)常温时,AlCl3溶液呈____性(填“酸”、“碱”或“中”),将AlCl3溶液蒸干,灼烧,得到的固体产物是________。AlCl3溶液和NaHCO3溶液混合时发生反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届临沂一模】二氧化氯(ClO2)是一种黄绿色易溶于水的气体,常用作饮用水消毒。实验室通过如下过程制备二氧化氯。

下列说法正确的是
A.电解时发生反应的离子方程式为NH4++3Cl-![]() 2H2↑+NCl3
2H2↑+NCl3
B.溶液X中大量存在的阴离子有Cl-、OH-
C.可用饱和食盐水除去ClO2中的NH3
D.可用明矾除去饮用水中残留的NaClO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)实验室制取少量溴乙烷的装置如下图所示。根据题意完成下列填空: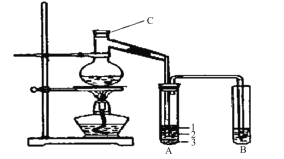
(1)装置图中C仪器的名称为 ,向C中加入的反应物是溴化钠、 和1:1的硫酸。配制体积比1:1的硫酸所用的定量仪器为 (选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
(2)写出加热时烧瓶中发生的主要反应的化学方程式 。
(3)将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是 。如图所示试管A中的物质分为三层,产物在第 层。
(4)试管A中除了产物和水之外,还可能存在 、 (写出化学式)。
(5)用浓的硫酸进行实验,若试管A中获得的有机物呈橙红色,除去其中杂质的最合理的方法是 (选填编号)。
a.蒸馏
b.氢氧化钠溶液洗涤
c.用四氯化碳萃取
d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称应该是 。
(6)实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:

(1)SO2对环境的危害主要是形成 。
(2)用Na2CO3溶液能吸收SO2的原因是 。
(3)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中发生如下反应:
①2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
②2NaHCO3+ SO2+H2O=2CO2↑+Na2SO3
③Na2SO3+ SO2+H2O=2NaHSO3
溶液中有关组分的质量分数变化如图是所示,图中的线2表示的组分为 (填化学式)。

(4)实验时,“反应II”中加入NaOH溶液的目的是 (用化学方程式表示)。
(5)获得的Na2SO3产品久置后质量变重,主要原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com