
| A. | H2A是弱酸 | |
| B. | 稀释0.1 mol/L H2A溶液,因电离平衡向右移动而导致c(H+)增大 | |
| C. | 在0.1 mol/L的H2A溶液中,c(H+)=0.12 mol/L | |
| D. | 若0.1 mol/L NaHA溶液中c(H+)=0.02 mol/L,则0.1 mol/L的H2A中c(H+)<0.12 mol/L |
分析 A.二元酸(H2A)在水中第一步电离为完全电离;
B.加水稀释电离平衡正移,但氢离子浓度减小;
C.二元酸(H2A)在水中的电离方程式为:H2A=H++HA-,HA-?H++A2-(Ka2=1.0×10-2),第一步完全电离,第二步部分电离,根据平衡常数计算溶液的c(H+);
D.H2A溶液中第一步电离出的氢离子,抑制了第二步电离.
解答 解:A.根据H2A=H++HA-可知,二元酸(H2A)在水中第一步电离为完全电离,则H2A酸性较强,不是弱酸,故A错误;
B.加水稀释电离平衡正移,但氢离子浓度减小,所以稀释0.1mol/L H2A溶液,电离平衡向右移动,c(H+)减小,故B错误;
C.二元酸(H2A)在水中的电离方程式为:H2A=H++HA-,HA-=H++A2-(Ka2=1.0×10-2),第一步完全电离,第二步部分电离,设电离的HA-为x,则:$\frac{(0.1+x).x}{0.1-x}$,解得:x=0.0084.所以在0.1mol•L-1的H2A溶液中,c(H+)=0.1mol/L+0.0084mol/L=0.1084mol/L,故C错误;
D.若0.1mol/L的NaHA溶液中c(H+)=0.02mol/L,0.1mol/L的H2A溶液中存在H2A═H++HA-,HA-?H++A2-,第一步电离出的氢离子,抑制了第二步电离,所以c(H+)<0.12mol/L,故D正确;
故选D.
点评 本题考查了弱电解质的电离平衡,涉及氢离子浓度的计算、电离常数的应用等知识,题目难度中等,注意该二元酸的电离特点,再结合守恒思想解答,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 0.02mol/(L•s) | B. | 0.04mol/(L•s) | C. | 0.06mol/(L•s) | D. | 0.03mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内每减少1mol A2,同时生成2mol AB3 | |
| B. | 容器内每减少1mol A2,同时生成3mol B2 | |
| C. | 容积一定时,容器内气体密度保持不变 | |
| D. | 容器内A2、B2、AB3的物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素和淀粉的组成都可用(C6H10O5)n表示,它们互为同分异构体 | |
| B. | 油脂的酸性条件下的水解叫皂化反应 | |
| C. | 将AlCl3溶液和Al2(SO4)3溶液分别蒸干灼烧,所得产物的成分均为Al2O3 | |
| D. | 由反应AgCl (s)+KI(aq)?AgI(s)+KCl(aq)可知Ksp(AgCl)>Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,反应类型:加聚反应(或聚合反应)
,反应类型:加聚反应(或聚合反应) 反应类型:取代反应
反应类型:取代反应查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏 | B. | 水洗后分液 | ||
| C. | 用过量饱和Na2CO3溶液洗涤后分液 | D. | 用过量NaCl溶液洗涤后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
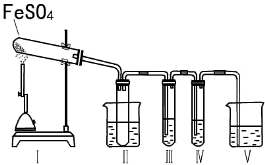
| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入KSCN溶液(或硫氰化钾溶液) | 溶液变成血红色 | 固体中含有Fe2O3 |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 固体中含有FeO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com