
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的原子序数依次增大。其中A元素原子的核外p电子数比s电子数少1。C是电负性最大的元素。D原子次外层电子数是最外层电子数2倍,E是第Ⅷ族中原子序数最小的元素。
(1)写出基态C原子的电子排布式_________________。
(2)A、B、C三种元素的第一电离能由大到小的顺序为______________(用元素符号表示),原因是___________________。
(3)已知DC4常温下为气体,则该物质的晶体类型是_________,组成微粒的中心原子的轨道杂化类型为____________,空间构型是___________。
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但AC3不易与Cu2+形成配离子,其原因是______________________。
(5)A、B两元素分别与D形成的共价键中,极性较强的是__________。A、B两元素间能形成多种二元化合物,其中与A3—互为等电子体的物质的化学式为__________。
(6)已知E单质的晶胞如图所示,则晶体中E原子的配位数为__________,一个E的晶胞质量为___________。

【答案】1s22s22p5F>N>ON 原子的2p 能级处于较稳定的半充满状态分子晶体sp3正四面体形由于电负性F>N>H,在NF3 分子中,共用电子对偏向F 原子,使得N 原子上的孤电子对难与Cu2+形成配位键Si-O 键N2O8112/NA g
【解析】
A元素原子的核外p电子数比s电子数少1,A的核外电子排布为:1s22s22p3,所以是氮元素,C是电负性最大的元素是氟元素,D原子次外层电子数是最外层电子数2倍,为硅元素,E是第Ⅷ族中原子序数最小的元素是铁元素,而A、B、C、D、E都是周期表中前四周期的元素,它们的原子序数依次增大,所以元素B是氧元素。
(1)C为F,基态C原子的电子排布式1s22s22p5。
(2)A、B、C三种元素的第一电离能由大到小的顺序为F>N>O (用元素符号表示),原因是N 原子的2p 能级处于较稳定的半充满状态故N>O,F最大。
(3)已知DC4即四氟化硅常温下为气体,则该物质的晶体类型是分子晶体,组成微粒的中心原子的轨道杂化类型为sp3,空间构型是正四面体形。
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但NF3分子中,共用电子对偏向F原子,使得N原子上孤电子对难与铜离子形成配位键,其原因是由于电负性F>N>H,在NF3 分子中,共用电子对偏向F 原子,使得N 原子上的孤电子对难与Cu2+形成配位键。
(5)A、B两元素分别与D形成的共价键中,O元素的非金属性大于N,则极性O-Si键>N-Si键;等电子体中原子个数相等及价电子数相等,N3-中含有3个原子、价电子数是16,与该离子互为等电子体的氮氧化物为N2O。
(6)该晶胞是体心立方晶胞,所以铁原子的配位数为8,该晶胞中Fe原子个数=1+8×1/8=2,体心上的Fe原子被顶点上的8个原子包围,所以其配位数是8,每个Fe原子的质量=M/NAg,则该晶胞质量就是两个Fe原子质量=2×M/NAg=2×56/NAg=112/NAg。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】随着化学工业的发展,各种化学合成材料已走进我们寻常百姓家,下列关于生活中常用材料的认识正确的是( )
A. 尼龙、羊毛和棉花都是天然纤维
B. 有机玻璃、锦纶、电玉、真丝巾都是合成塑料
C. 天然橡胶的化学组成是聚异戊二烯
D. 装食品用的聚乙烯塑料可以通过加热进行封口
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱溶液中都含有OH-,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊试液变蓝色B.能与盐酸反应生成水
C.能与Na2S04溶液反应生成BaS04沉淀D.能与CO2反应生成水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D 原子序数依次增大且最外层电子数之和为17。B、D 同主族,短周期中C原子半径最大,B最外层电子数是次外层的3倍。下列推断不正确的是
A. 元素B、C、D 形成的化合物的水溶液呈中性
B. 元素B、C 形成的化合物中可能既含有离子键又含共价键
C. 离子半径从大到小的顺序为D>B>C
D. 元素B 的简单气态氢化物的热稳定性比D 的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①假设用酸性高锰酸钾溶液吸收煤燃烧产生的SO2,该过程中高锰酸根被还原为Mn2+,请写出该过程的离子方程式______________。
②将燃煤产生的二氧化碳加以回收,可降低碳的排放。左图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图,a电极名称:_____________(填“正极”或“负极”),b电极的反应式:________________________。

(2)如果采用NaClO、Ca(ClO)2作吸收剂,也能得到较好的烟气脱硫效果。
已知下列反应:
SO2(g)+2OH-(aq) ==SO32-(aq)+H2O(l) ΔH1
ClO-(aq)+SO32-(aq) ==SO42-(aq)+Cl-(aq) ΔH2
CaSO4(s)==Ca2+(aq)+SO42-(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO-(aq) +2OH-(aq) = CaSO4(s) +H2O(l) +Cl-(aq)的ΔH=_____。
II.(3)FeO42-在水溶液中的存在形态如图所示。

①若向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数的变化情况是__________。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,_________转化为_________(填微粒符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的利用是国际社会普遍关注的问题。
(1)CO2的电子式是__________
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
![]()
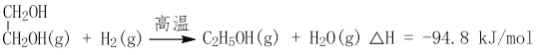
获取乙二醇的反应历程可分为如下2步:
I. 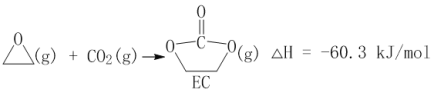
II.EC加氢能生成乙二醇与甲醇。
①步骤II的热化学方程式是__________;
②研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
反应温度/℃ | EC转化率/ % | 产率/% | |
乙二醇 | 甲醇 | ||
160 | 23.8 | 23.2 | 12.9 |
180 | 62.1 | 60.9 | 31.5 |
200 | 99.9 | 94.7 | 62.3 |
220 | 99.9 | 92.4 | 46.1 |
由上表可知,温度越高,EC的转化率越高,原因是__________。温度升高到220℃时,乙二醇的产率反而降低,原因是__________
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极 a 接电源的__________极(填“正”或“负”),生成甲醇的电极反应式是__________
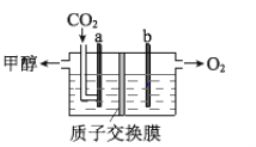
(4)CO2较稳定、能量低。为实现CO2的高效使用,下列研究方向合理的是__________(填序号)。
a.降低CO2参与反应的速率和比例
b.利用电能、光能或热能预先活化CO2分子
c.选择高效的催化剂降低反应条件
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验发现,298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( )
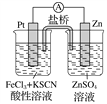
A. 该原电池的正极反应是Zn-2e-===Zn2+
B. 左烧杯中溶液的血红色逐渐褪去
C. 该电池铂电极上有气泡出现
D. 该电池总反应为3Zn+2Fe3+===2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中能大量共存的一组离子是( )
A. K+、H+、SO32-、S2- B. NH4+、K+、OH-、Cl-
C. H+、K+、MnO4-、SO42- D. Fe3+、Na+、S2-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的叙述正确的是
A. 中和滴定实验中指示剂不宜加入过多,通常控制量在1 mL ~2mL
B. 用50mL酸式滴定管可准确量取25.00mLKMnO4 溶液
C. 用量筒量取5.00mL1.00mol·L-1 盐酸
D. 中和滴定实验中的锥形瓶用待测液润洗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com