
【题目】氨气是工农业生产中不可或缺的物质,研究制取氨气的机理意义非凡。
(1)在常温、常压、光照条件下,N2在掺有少量Fe2O3的TiO2催化剂表面与水发生下列反应:
N2(g)+3H2O(l)![]() 2NH3(g)+
2NH3(g)+![]() O2(g) △H=a kJ mol-1 。
O2(g) △H=a kJ mol-1 。
为进一步研究生成NH3的物质的量与温度的关系,常压下达到平衡时测得部分实验数据如下:
T/K | 303 | 313 | 323 |
n(NH3)/(l0-2 mol) | 4.8 | 5.9 | 6.0 |
此反应的a_________0,△S________0。(填“>”“<”或“ = ”)
(2)—定温度和压强下,在2 L的恒容密闭容器中合成氨气:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。
2NH3(g) △H=-92.4 kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。
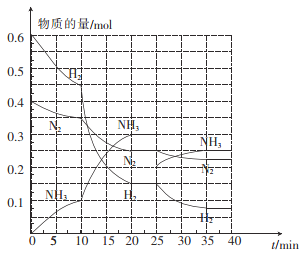
① 0~10 min内,以NH3表示的平均反应速率为_________。
② 在10~20 min内,NH3浓度变化的原因可能是_______。
A.加入催化剂 B.缩小容器体积 C.降低温度 D.增加NH3的物质的量
③ 在反应进行至25 min时,曲线发生变化的原因是____________,达到第二次平衡时,新平衡的平衡常数K2______K1(填“>”“<”或“ = ”)
【答案】(1)> ;>
(2)①0.005 mol L-1 min-1
②BC
③移走 0.1 molNH3 ; =
【解析】
试题分析:(1)升高温度NH3的物质的量最多,所以N2(g)+3H2O(l) ![]() 2NH3(g)+
2NH3(g)+![]() O2反应吸热,a>0;反应后气体物质的量增多,△S>0;(2)① 0~10 min内,以NH3表示的平均反应速率为
O2反应吸热,a>0;反应后气体物质的量增多,△S>0;(2)① 0~10 min内,以NH3表示的平均反应速率为![]()
![]() 0.005 mol L-1 min-1;② 在10~20 min内,NH3浓度逐渐增大,变化的原因可能是A.加入催化剂,平衡不移动,NH3物质的量不变,A错误; B.缩小容器体积,平衡正向移动,氨气的物质的量增大,B正确 ; C.降低温度,平衡正向移动,NH3物质的量增大,C正确; D.增加NH3的物质的量,平衡逆向移动,氮气、氢气增多,D错误;③ 在反应进行至25 min时,氨气的物质的量突然由0.3mol变为0.2mol,曲线发生变化的原因是移走 0.1 molNH3,平衡常数只与温度有关,温度不变平衡常数不变,达到第二次平衡时,新平衡的平衡常数K2=K1。
0.005 mol L-1 min-1;② 在10~20 min内,NH3浓度逐渐增大,变化的原因可能是A.加入催化剂,平衡不移动,NH3物质的量不变,A错误; B.缩小容器体积,平衡正向移动,氨气的物质的量增大,B正确 ; C.降低温度,平衡正向移动,NH3物质的量增大,C正确; D.增加NH3的物质的量,平衡逆向移动,氮气、氢气增多,D错误;③ 在反应进行至25 min时,氨气的物质的量突然由0.3mol变为0.2mol,曲线发生变化的原因是移走 0.1 molNH3,平衡常数只与温度有关,温度不变平衡常数不变,达到第二次平衡时,新平衡的平衡常数K2=K1。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】反应A (g)+3B (g)![]() 2C (g)+2D (g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是
2C (g)+2D (g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是
A. υ (A)=0.05mol/(Ls) B. υ (B)=0.06mol/(Lmin)
C. υ (C)=0.04mol/(Ls) D. υ (D)=0.03mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性。下列关于锂的判断可能正确的是
A.Li能在空气中燃烧B.Li2O熔点较低
C.Li2CO3能溶于水D.LiOH受热时不易分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊.A受热分解的化学方程式为 .
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复到室温,向所得溶液中各滴入2滴酚酞溶液. ①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论: .
②同学们在两烧杯中还观察到以下现象.其中,盛放Na2CO3的烧杯中出现的现象是(填字母序号).
a.溶液温度下降b.溶液温度升高c.滴入酚酞后呈浅红色d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中. 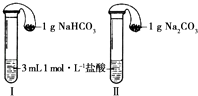
①两试管中均产生气体,(填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈.
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是(填字母序号).
a.装置Ⅰ的气球体积较大b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成0.5molL﹣1的溶液,设计如下方案并对反应现象做出预测:
实验方案 | 预测现象 | 预测依据 |
操作1:向2mL Na2CO3溶液中滴加1mL 0.5molL﹣1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32﹣浓度较大,能与CaCl2发生反应:(写离子方程式) |
操作2:向2mL NaHCO3溶液中滴加1mL 0.5molL﹣1 CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32﹣浓度很小,不能与CaCl2反应 |
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体,则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1molOH﹣的质量为17gmol﹣1
B.0.5mol H2所占体积约为11.2L
C.等质量的金刚石和晶体硅所含原子个数之比为7:3
D.1mol NaCl固体溶于0.5L水中,所得溶液的物质的量浓度为2molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下:
弱酸 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)CH3COOH、H2CO3、H2SO3三种酸中酸性最弱的是__________(填化学式)。
(2)CH3COOH的电离平衡常数表达式为K=__________。
(3)写出H2CO3的第二步电离方程式:_____________。
(4)写出H2SO3溶液和CH3COONa溶液反应的离子方程式:____________________。
(5)将体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH的变化如图所示,则HX的电离平衡常数____________(填“大于”“ 小于”或“等于”)醋酸的电离平衡常数,理由是__________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Fe(OH)3胶体和MgCl2溶液性质叙述正确的是
A. 均能够产生丁达尔效应 B. 微粒直径均在1~100 nm之间
C. 分散质微粒均可透过滤纸 D. 加入少量NaOH 溶液,只有MgCl2溶液产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一定温度下有:a.盐酸 b.硫酸 c.醋酸三种酸溶液.(用序号abc填空)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是__________.
②当其pH相同时,物质的量浓度由大到小的顺序为_________.将其稀释10倍后,pH由大到小的顺序为_____________
(2)某温度下,纯水中的c (H+)= 4.0×10-7 mol/L, 则此温度下纯水中的c (OH-)=______________mol/L; 若温度不变, 滴入稀NaOH溶液, 使c (OH-)= 5.0×10-6 mol/L,则溶液的c (H+)= _________________mol/L.
(3)在25℃时,100ml 1.0mol/L的盐酸与等体积1.2mol/L的氢氧化钠溶液混合, 混合后溶液的pH= _______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度小于1×10-6mol·L-1),需调节溶液pH范围为
A. (3.5 , 5.0) B. (3.5 , 7.1)
C. (5.0 , 7.1) D. ( 4.0 , 7.1)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com