
| A. | 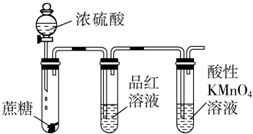 检验浓硫酸与蔗糖反应产生的二氧化硫 | |
| B. | 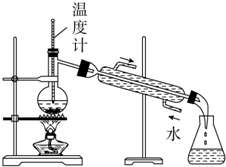 分离甲苯和水 | |
| C. | 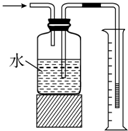 测量氨气的体积 | |
| D. | 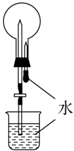 进行二氧化碳喷泉实验 |
分析 A.浓硫酸具有脱水性,使蔗糖脱水后,C与浓硫酸反应生成二氧化碳、二氧化硫,二氧化硫具有漂白性、还原性;
B.蒸馏时测定馏分的温度,冷却水下进上出;
C.氨气极易溶于水;
D.二氧化碳在水中的溶解度不大.
解答 解:A.浓硫酸具有脱水性,使蔗糖脱水后,C与浓硫酸反应生成二氧化碳、二氧化硫,二氧化硫具有漂白性、还原性,则图中品红褪色、高锰酸钾褪色可检验浓硫酸与蔗糖反应产生的二氧化硫,故A正确;
B.蒸馏时测定馏分的温度,冷却水下进上出,则温度计的水银球应在烧瓶支管口处,冷水方向下进上出,故B错误;
C.氨气极易溶于水,则不能利用排水法测定氨气的体积,故C错误;
D.二氧化碳在水中的溶解度不大,则图中不能形成喷泉,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、混合物分离提纯、实验装置的作用等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:解答题
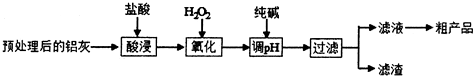
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 2.8 |
| A13+ | 3.4 | 4.7 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子 | 要求 |
| A | K+、Cl-、SO42-、MnO4- | c(K+)<c(Cl-) |
| B | Na+、Ca2+、I-、NO3- | c(H+)/c(OH-)=1×1014 |
| C | Al3+、NH4+、SO42-、CH3COO- | 滴加NaOH溶液立刻有气体产生 |
| D | Na+、Mg2+、Ag+、NO3- | 滴加氨水先有沉淀产生,后沉淀部分溶解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
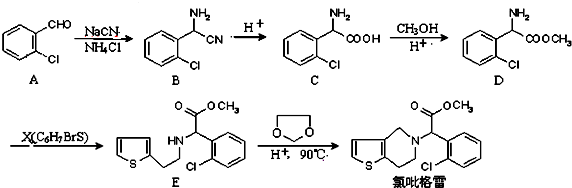
 .
. .
.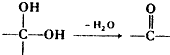
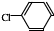 中氯原子较难水解
中氯原子较难水解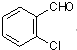 )可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式
)可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式 、
、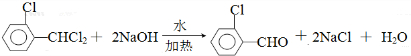 .该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式
.该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式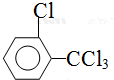 、
、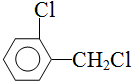 .
.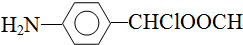 .
.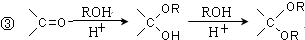
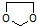 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: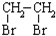
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 | |
| B. | Y元素最高价氧化物对应的水化物化学式为H2YO4 | |
| C. | 原子半径由大到小的顺序为Z>Y>W | |
| D. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过量石灰乳吸收工业尾气中的SO2:Ca2++2OH-+SO2═CaSO3↑+H2O | |
| B. | 用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解NaCl溶液:2C1-+2H2O$\frac{\underline{\;高温\;}}{\;}$H2↑+Cl2↑+2OH- | |
| D. | 将Fe2O3加入到HI溶液中:Fe2O3+6H+═2Fe3++3H2O↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
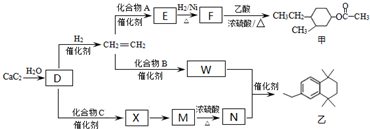
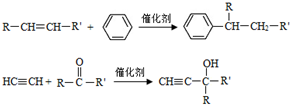 (-R、-R′代表烃基或-H)
(-R、-R′代表烃基或-H)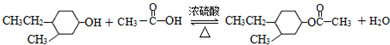 .
.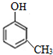 .
.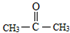 .
.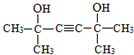 .
.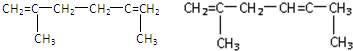 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,相同浓度的盐酸与氨水的混合溶液的pH=7,消耗盐酸的体积大 | |
| B. | 将pH=5的醋酸溶液稀释1000倍,溶液的pH=8 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com