
【题目】具有真正意义上的元素周期表是由哪位化学家发现的( )
A. 门捷列夫(俄国) B. 纽兰兹(英国)
C. 迈尔(德国) D. 尚古多(法国)
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种烃,具有下列性质:
①各取0.1mol分别充分燃烧,其中B、C、E燃烧所得的CO2均为4.48L(标准状况),A和D燃烧所得的CO2都是前三者的3倍;
②在适宜条件下,A、B、C都能跟氢气发生加成反应,其中A可以转化为D、B可以转化为C,C可以转化为E;
③B和C都能使溴水或酸性KmnO4溶液褪色,而A、D、E无此性质;
④用铁屑作催化剂时,A可与溴发生取代反应.
判断A、B、C、D、E各是什么物质,写出结构简式ABCDE .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.构成原电池正极和负极的材料必须是两种金属
B.由Cu、Zn作电极与CuSO4溶液组成的原电池中Cu是负极
C.马口铁(镀锡铁)破损时与电解质溶液接触,锡先被腐蚀
D.铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是重要的有机溶剂和化工原料,下图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品。请回答:

(1)有机物A中含有的官能团名称是____________。
(2)写出反应①的化学方程式_____________。
(3)已知反应②在催化剂作用下无需加入其他反应物即可一步合成产物,同时生成一种无色无味气体,该气体的化学式为_________。
(4)下列说法正确的是_________。
A.可以用氢氧化钠溶液除去乙酸乙酯中混有的A
B.C→B、B→A的氧化剂可以相同,也可以不同
C.反应③是①、②、③中唯一符合绿色化学的“零排放”要求的
D.反应①~④中至少涉及到取代反应、加成反应、氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向l00 mL0.1 mol·L-1 硫酸铝铵[NH4A1(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。 随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是
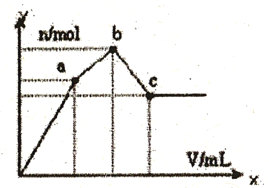
A. a点的溶液呈中性
B. c点溶液呈碱性
C. c点加入Ba(OH)2溶液的体积为200 mL
D. b 点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-= Al(OH)3↓+2BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期的三种元素X,Y,Z,原子序数依次增大.X,Y,Z元素原子的核外电子层数之和是6,X元素原子核内无中子,Y元素原子的最外层电子数是其电子层数的2倍,Z元素原子最外层电子数为7.
(1)Y元素在周期表中周期族;Z元素的原子结构示意图是
(2)仅由X元素与Y元素形成的化合物称为;化合物XZ的电子式是;
(3)Z元素的单质与NaOH溶液反应的离子方程式为
(4)Z元素的单质与大气污染物(SO2)在水溶液中反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,将224 L HC1气体溶于635 mL水中,所得盐酸的密度为1.18g·cm-3。试计算:
①取出这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是________。
②在40.0 mL 0.065 mol·L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过________mL。
(2)配制0.80 mol·L-1 NaOH溶液475 mL,回答下列问题:
①根据计算用托盘天平称取NaOH的质量为____g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度____0.80 mol·L-1(填“大于”、“等于”或“小于”,下同)。若还未等溶液冷却就定容了,则所得溶液浓度_____0.80 mol·L-1 。
②0.80 mol·L-1 NaOH溶液质量分数和等质量的水混合溶液浓度 _____0.40 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若某原电池的离子方程式是Zn+Cu2+=Zn2++Cu,则该原电池的构成是( )
正极 | 负极 | 电解质溶液 | |
A | Cu | Zn | HCl |
B | Zn | Cu | CuSO4 |
C | Cu | Zn | CuSO4 |
D | Cu | Zn | ZnCl2 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com