
【题目】漂白粉是由氯气通入石灰乳制得,漂白粉的成分是CaCl2、Ca(ClO)2及少量Ca(OH)2,其中有效成分中氯元素的化合价是( )
A.-2价B.-1价C.+1价D.+3价
科目:高中化学 来源: 题型:
【题目】对已达到平衡的反应4NH3(g)+6NO(g)5N2(g)+6H2O( g) 减小压强,产生的影响是
A.正、逆反应速率都减小,平衡向正反应方向移动
B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
D.正、逆反应速率都增大,平衡不发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是一种新型的化学电源,其构造如图一所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
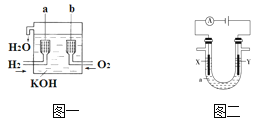
(1)a电极反应式是_______________________;
(2)该燃料电池生成了360 kg的水,则电路中通过了_____________mol的电子。
(3)用如图二所示电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极反应式是___________________。
②Y电极的材料是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是近年来我国化石燃料和其他能源的消耗构成示意图,下列说法正确的是( )
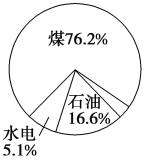
A. 当今人类所需的能量绝大部分是由化学反应产生的
B. 煤、石油、天然气的成分都是烃
C. 为消除温室效应,应禁用煤、石油、天然气等含碳能源
D. 核能、氢能、太阳能是当今社会的主要能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 把煤隔绝空气加强热使之分解的过程叫干馏
B. 煤的干馏包含着物理变化和化学变化
C. 煤中含有大量苯和甲苯,可以用先干馏后分馏的方法将其分离开
D. 以煤为主要原料,可以合成甲醇等液体燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
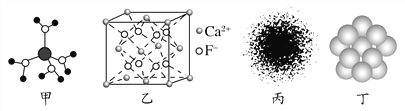
A. 水合铜离子的模型如图甲所示,1个水合铜离子中有4个配位键
B. CaF2晶体的晶胞如图乙所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图丙所示,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图丁所示,为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
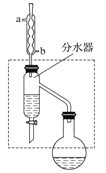
【题目】乙酸丁酯是重要的化工原料,具有水果香味。实验室制备乙酸丁酯(CH3COOCH2CH2CH2CH3)的反应装置示意图和有关信息如下:
乙酸 | 正丁醇 | 乙酸丁酯 | |
熔点/℃ | 16.6 | -89.5 | -73.5 |
沸点/℃ | 117.9 | 117 | 126.0 |
密度/g·cm-3 | 1.1 | 0.80 | 0.88 |
(1)乙酸丁酯粗产品的制备
在干燥的50 mL圆底烧瓶中,装入沸石,加入12.0 mL正丁醇和16.0 mL冰醋酸(过量),再加3~4滴浓硫酸。然后再安装分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管,然后小火加热。写出制备乙酸丁酯的化学方程式_________。将烧瓶中反应后的混合物冷却与分水器的酯层合并。装置中冷水应从________(填“a”或“b”)口通入;通过分水器不断分离除去反应生成的水的目的是_____________。(2)乙酸丁酯的精制
将乙酸丁酯粗产品用如下的操作进行精制:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤。①正确的操作步骤是________________(填标号)。
A.①②③④ B.③①④② C.④①③② D.③④①②
②在乙酸丁酯的精制中,用10%碳酸钠洗涤的主要目的是_________。
③在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸丁酯从分液漏斗的上口倒出
b.直接将乙酸丁酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出
(3)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8 mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验方法或试剂不能达到实验目的的是
A.鉴别SO2和CO2气体:用酸性KMnO4溶液
B.证明溶液中含有NH4+:用浓氢氧化钠溶液和蓝色石蕊试纸
C.鉴别Br-和I-:用过氧化氢溶液和淀粉溶液
D.鉴别NO2和溴蒸气:用蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是( )
A.由2H和18O所组成的水22g,其中所含的中子数为12 NA
B.分子数为NA的N2、CO混合气体体积在标况下为22.4 L,质量为28 g
C.标准状况下,22.4LNO和11.2L O2混合后气体的分子总数为NA
D.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com