
下列装置中,Fe腐蚀由快到慢的顺序为 ( )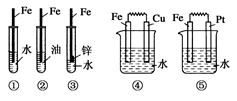
| A.⑤④③②① | B.⑤④①②③ | C.⑤③④①② | D.①②④③⑤ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届江苏省高二上学期期中考试化学试卷(选修)(解析版) 题型:选择题
下列装置中,Fe腐蚀由快到慢的顺序为( )
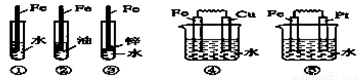
A. ⑤④③②① B. ⑤④①②③ C. ⑤③④①② D. ①②④③⑤
查看答案和解析>>
科目:高中化学 来源:2014届云南省高二第二次月考(6月)化学试卷(解析版) 题型:选择题
下列装置中,Fe腐蚀由快到慢的顺序为( )
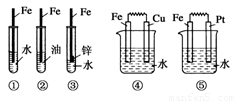
A.⑤④③②①
B.⑤④①②③
C.⑤③④①②
D.①②④③⑤
查看答案和解析>>
科目:高中化学 来源:2014届辽宁省分校高二12月月考化学试卷(解析版) 题型:选择题
下列装置中,Fe腐蚀由快到慢的顺序为 ( )
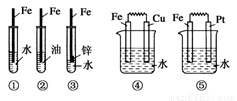
A.⑤④③②① B.⑤④①②③ C.⑤③④①② D.①②④③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com