
| A. | 铝能置换出氧化铁中的铁,钢铁工业利用铝热反应冶炼铁 | |
| B. | 用铝制容器盛放浓硝酸,是因为铝和浓硝酸不反应 | |
| C. | 明矾溶于水生成氢氧化铝胶体,起消毒杀菌的作用 | |
| D. | 因为液态氨气化时吸热,可用液态氨作制冷剂 |
分析 A.铝能置换出氧化铁中的铁,发生铝热反应,钢铁工业炼铁是利用还原法得到,一氧化碳还原氧化铁得到金属铁;
B.常温下能用铝制容器盛放浓硝酸和浓硫酸,是因为反应生成了致密的氧化膜阻止进一步反应;
C.明矾可用于净水,是因为明矾溶于水生成胶状物可吸附悬浮于水中的杂质;
D.液氨汽化时要吸收大量的热,使温度降低.
解答 解:A.能置换出氧化铁中的铁,发生铝热反应,可以用来焊接钢轨,钢铁工业炼铁是利用还原法得到,一氧化碳还原氧化铁得到金属铁,故A错误;
B.常温下能用铝制容器盛放浓硝酸和浓硫酸,是因为反应生成了致密的氧化膜阻止进一步反应,故B错误;
C.明矾溶于水生成胶状物可吸附悬浮于水中的杂质,不能除掉可溶性杂质和细菌等,不能起消毒杀菌的作用,故C错误;
D.液氨汽化时要吸收大量的热,使温度降低,可用作制冷剂,故D正确;
故选D.
点评 本题考查液氨、铝的钝化、明矾净水、铝热反应、工业炼铁等原理等,题目难度不大,注意明矾溶于水生成胶状物可吸附悬浮于水中的杂质,不能除掉可溶性杂质和细菌等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用10ml量筒量取7.5ml稀盐酸 | |
| B. | 用托盘天平称取25.20gNaCl晶体 | |
| C. | 用蒸发结晶的方法由硫酸铜溶液制取蓝帆 | |
| D. | 用100ml容量瓶配置0.5mol/l的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
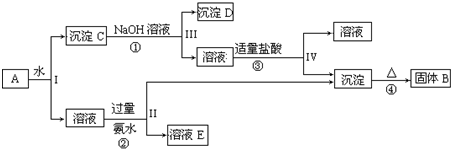
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
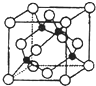 周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增.R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子.工业上通过分离液态空气获得X单质.Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和.Z基态原子的最外能层只有一个电子,其他能层均已充满电子.
周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增.R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子.工业上通过分离液态空气获得X单质.Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和.Z基态原子的最外能层只有一个电子,其他能层均已充满电子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将该Na2CO3 溶液转移至250ml容量瓶中,加蒸馏水稀释至刻度线,摇匀 | |
| B. | 将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取150ml蒸馏水加入,搅拌 | |
| C. | 将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取400ml蒸馏水加入,搅拌 | |
| D. | 将该Na2CO3 溶液转移至500ml容量瓶中,加蒸馏水稀释至刻度线,摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com