
【题目】按要求完成下列问题。
Ⅰ.煅烧硫铁矿(主要成分为FeS2)的反应为:
4FeS2+11O2 ![]() 2Fe2O3+8SO2。试回答下列问题。
2Fe2O3+8SO2。试回答下列问题。
(1)可用哪些物质来表示该反应的化学反应速率__________ 。
(2)某时刻时测得,生成SO2的速率为0.64 mol/(Ls),则氧气减少的速率为_______ mol/(Ls)。
(3)该工业生产中将矿石粉碎的目的:
。
Ⅱ.当运动员肌肉受伤时,队医会随即对准运动员的受伤部位喷射药剂氯乙烷,进行局部冷冻麻醉处理。
(1)制取氯乙烷 (CH3CH2Cl)的最好的方法是 。
a.乙烷与氯气发生取代反应
b.乙烯与氯气发生加成反应
c.乙烷与氯化氢反应
d.乙烯与氯化氢发生加成反应
(2)写出所选反应的化学方程式: 。
Ⅲ.某钢铁厂高炉炼铁的主要反应过程如下:
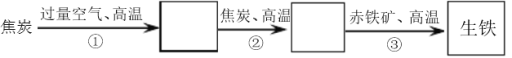
(1)写出步骤②③的化学方程式:
② ;
③ 。
(2)下列有关高炉炼铁的说法正确的是 。
a.增加高炉的高度可以提高CO的利用率
b.三个反应均为吸热反应
c.从高炉炉顶出来的气体中含有没有利用的CO气体
d.只有步骤②的反应是可逆反应
【答案】Ⅰ.(1)SO2和O2
(2)0.88
(3)增大接触面积,加快反应速率
Ⅱ.(1)d
(2)CH2=CH2+HCl![]() CH3CH2Cl
CH3CH2Cl
Ⅲ.(1)②CO2+C![]() 2CO ③Fe2O3+3CO
2CO ③Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
(2)c
【解析】
试题分析:Ⅰ.(1)在反应4FeS2+11O2 ![]() 2Fe2O3+8SO2中,FeS2和Fe2O3属于固态物质,不能用来表示化学反应速率,可用O2和SO2来表示该反应的化学反应速率。
2Fe2O3+8SO2中,FeS2和Fe2O3属于固态物质,不能用来表示化学反应速率,可用O2和SO2来表示该反应的化学反应速率。
(2)根据化学反应方程式可知,某时刻时测得,生成SO2的速率为0.64 mol/(Ls),则氧气减少的速率为v(O2)=![]() v(SO2)=
v(SO2)=![]() ×0.64 mol/(Ls)=0.88mol/(Ls)。
×0.64 mol/(Ls)=0.88mol/(Ls)。
故答案为:0.88mol/(Ls);
(3)该工业生产中将矿石粉碎的目的: 增大接触面积,加快反应速率。
故答案为:增大接触面积,加快反应速率;
Ⅱ.(1)A.乙烷与氯气发生取代反应:CH3CH3+Cl2→CH3CH2Cl+HCl,该反应有杂质HCl生成,所以不符合原子经济的理念,故A错误;B.乙烯与氯气发生加成反应:CH2=CH2+Cl2→CH2ClCH2Cl,产物是二氯乙烷不是氯乙烷,故B错误;C.乙烷与氯气发生取代反应,得不到氯乙烷,是多种卤代烃的混合物,故C错误;D.乙烯与氯化氢发生加成反应:CH2=CH2+HCl→CH3CH2Cl,生成物只有氯乙烷,符合原子经济理念,故D正确。
故答案为:D;
(2)乙烯和氯化氢在一定条件下发生加成反应生成氯乙烷,方程式为:CH2=CH2+HCl![]() CH3CH2Cl。
CH3CH2Cl。
故答案为:CH2=CH2+HCl![]() CH3CH2Cl;
CH3CH2Cl;
Ⅲ.(1)高炉炼铁的流程为:焦炭与过量空气在高温条件下生成二氧化碳,二氧化碳又与焦炭在高温条件下生成一氧化碳,最终一氧化碳把赤铁矿中的铁还原出来。发生反应为:
①C+O2![]() CO2、②CO2+C
CO2、②CO2+C![]() 2CO、③3CO+Fe2O3
2CO、③3CO+Fe2O3![]() 2Fe+3CO2。
2Fe+3CO2。
故答案为:②CO2+C![]() 2CO、③3CO+Fe2O3
2CO、③3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(2)a.化学反应达到平衡状态后,反应混合物中各组分含量不再发生变化。所以,增加高炉的高度CO的利用率不变,故a错误;b.反应①③为放热反应、反应②为吸热反应,故b错误;c.化学反应3CO+Fe2O3![]() 2Fe+3CO2属于可逆反应,所以从高炉炉顶出来的气体中含有没有利用的CO气体,故c正确; d.步骤②③的反应均是可逆反应,故d错误。
2Fe+3CO2属于可逆反应,所以从高炉炉顶出来的气体中含有没有利用的CO气体,故c正确; d.步骤②③的反应均是可逆反应,故d错误。
故答案为:c。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.1 mol CH3+含电子数为10NA
B.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA
C.标准状况下,22.4 L水中含有原子总数为3NA
D.1molCl2完全溶于水后,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)在一密闭容器中一定量A、B的混合气体发生反应:aA(g)+bB(g) ![]() cC(s)+dD(g),平衡时测得A的浓度为0.60 mol/L,保持温度不变,将容器的容积扩大到原来的3倍,再达平衡时,测得A的浓度降为0.20 mol/L。下列有关判断一定正确的是
cC(s)+dD(g),平衡时测得A的浓度为0.60 mol/L,保持温度不变,将容器的容积扩大到原来的3倍,再达平衡时,测得A的浓度降为0.20 mol/L。下列有关判断一定正确的是
A.平衡向正反应方向移动 B.A的转化率增大
C.D的体积分数增大 D.a+b<c+d
(2)①25 ℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
HSO3-的电离平衡常数表达式K=__________________。
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为:_______________。
③根据H2SO3的电离常数数据,判断NaHSO3溶液显酸性还是显碱性?
Ⅱ.0.98 gCu(OH)2样品受热分解的热重曲线(样品质量随温度变化的曲线)如图所示。

请回答下列问题:
(1)试确定1 100 ℃时所得固体B的化学式(要求写出推理或计算过程)。
(2)固体A在一定条件下能与一种能使湿润的红色石蕊试纸变蓝的气体反应,得到红色固体单质和气体单质,则该反应的化学方程式为:____________________;若反应中转移0.015 mol电子,则消耗还原剂的物质的量为________________。
(3)取少量固体B于试管中,加入足量的稀硫酸得到蓝色溶液,同时观察到试管中还有红色固体存在,该反应的离子方程式为:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于取代反应的是
A.用日光照射甲烷与氯气的混合气体
B.乙烯通入溴水中
C.在FeBr3作催化剂的条件下,苯与液溴反应
D.乙醇与乙酸的酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示。下列结论错误的是

A.反应开始2 min内平均反应速率最大
B.反应4~6 min内平均反应速率最小
C.反应开始4 min内温度对反应速率的影响比浓度大
D.反应在第2 min到第4 min间生成CO2 的平均反应速率最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.硫酸可用于精炼石油、金属加工之前的酸洗
B.氨易液化,常用作制冷剂
C.二氧化硫可用来加工食品,以使食品增白
D.硅是半导体材料,用作光电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将7.28g Fe溶于过量的稀H2SO4中,在加热的条件下,用2.02gKNO3去氧化溶液中Fe2+,待反应完全后,剩余Fe2+还需0.4mol/L KMnO4溶液25mL才能完全氧化,则KNO3的还原产物
A.NO B.NO2 C.N2O D.N2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类或归类正确的是( )
A.化合物:CaCl2、烧碱、聚乙烯、HD
B.酸性氧化物:SO2、NO、CO2、Mn2O7
C.胶体:雾、牛奶、豆浆、烟水晶
D.同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】6月26日是国际禁毒日,据公安部通报,目前冰毒、摇头丸、氯胺酮等新型毒品在我国有较大传播范围,吸、贩新型毒品问题十分突出。已知下列四种毒品的结构简式:

下列说法不正确的是( )
A.冰毒能与盐酸反应
B.摇头丸具有两性
C.1molK粉最多可以与4molH2发生加成反应
D.适当条件下,1mol大麻最多可与3mol Br2发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com